Wie rechnet man N von 10gramm und m einer stoffportion mit 1,5 mol teilchen aus?
Chemie
2 Antworten
Folgende Formel brauchst du:
m=n*M (m=Masse, n=Stoffmenge, M=molare Masse)
N=NA * n (N=Teilchenzahl, NA=Avogadro Konstante, n=Stoffmenge)
Gegebenenfalls musst du die Formeln umstellen.
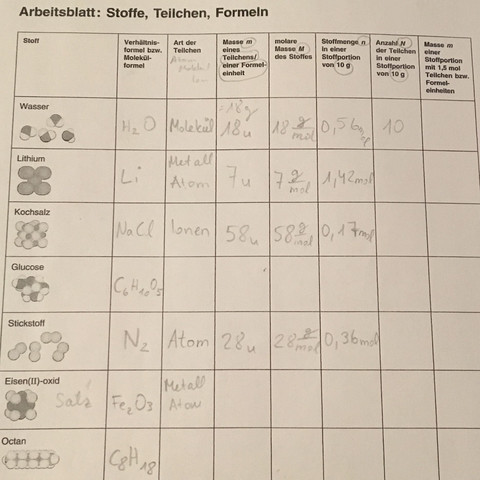
1) Formeln: Diese sind für Glucose und Eisen(II)-oxid von Dir falsch angegeben. Suche im Internet nach den richtigen Formeln.
2) Art der Teilchen: Wenn Du bei Stickstoff die Formel N₂ angibst, dann liegen doch sicher keine Atome vor. Bei Eisen(II)-oxid liegt kein Metall vor (und für Sauerstoff auch kein Nichtmetall). Es liegt der gleiche Bindungstyp wie im Natriumchlorid vor.
3) Die Masse m hast Du bis auf die des Wassers, denn hier stehen zwei Massen, richtig angegeben.
4) Die molare Masse M ist überall richtig.
5) Die Stoffmenge n stimmt bei Deinen Berechnungen.
6) Hier gilt als Voraussetzung die Aussage von AVOGADRO:
In der Stoffmenge n = 1 mol eines jeden Systems ist die Anzahl der Teilchen gleich. Man konnte diese ermitteln, und sie beträgt N = 6,022•10²³ Atome (oder Moleküle).
Achtung! Da nach der Zahl der Teilchen gefragt ist, musst Du bei den Ionenverbindungen aufpassen (warum?).
Du musst doch nur zwei Werte in den Taschenrechner mit einem "mal" dazwischen eingeben. Hattet ihr noch kein Mathe in der Schule?
Ich kann mit der formel nichts anfangen :(