Was ist hier anzukreuzen (Chemie, Batterie)?
Zink gehört zum Minuspol.
Zink gehört zum Pluspol.
Kupfer gehört zum Pluspol.
Kupfer gehört zum Minuspol.
1 Antwort

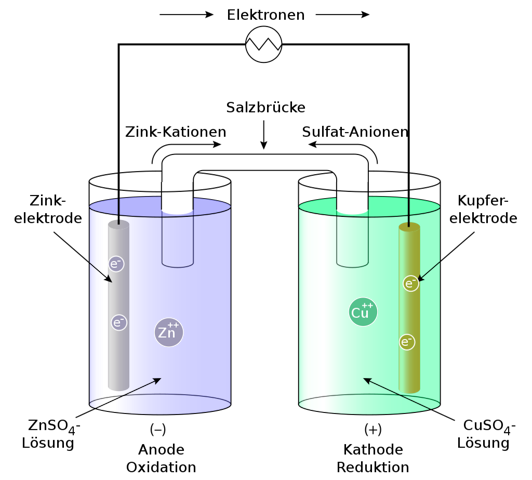
Bei den hier beschriebenen Elektrodenkombination handelt es sich um ein Daniell-Element, welches aus einer Halbzelle mit einer Zinkelektrode und beispielsweise einer Zink(II)sulfat-Lösung und einer Halbzelle mit einer Kupferelektrode und einer Kupfer(II)sulfat-Lösung besteht.
Da Zink wesentlich unedler ist als Kupfer, wird dieses oxidiert und gibt seine Elektronen ab. Es stellt somit die Anode (hier: Minuspol) dar. Kupfer ist wesentlich edler als Zink, weswegen die Kupfer(II)Ionen aus der Lösung an der Kupferelektrode reduziert werden. Dabei handelt es sich die Kathode (hier: Pluspol).
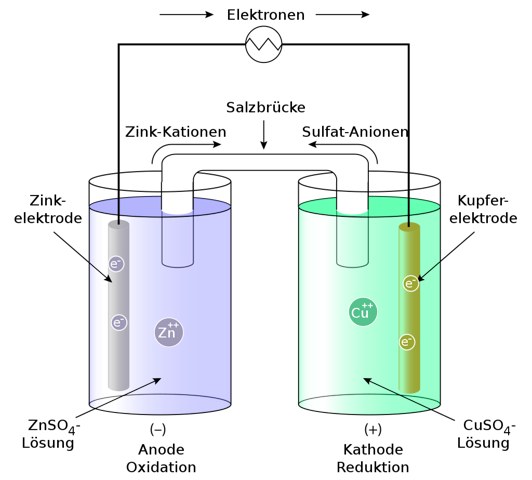
(Urheber: Von Rehua - Eigenes Werk, CC BY 3.0, https://commons.wikimedia.org/w/index.php?curid=17902682)
~Johannes