Warum ist die Verhältnisformel Na+Cl-?
Ich dachte es gibt da diese HonClbrief regel,dass die Elemente dieser Buchstaben immer nur als Moleküle vorkommen. Ist das hier ein Unterschied,weil es Ionen und keine Elemente sind?
Außerdem wollte ich noch fragen: Was genau ist mit Salzkristall gemeint?
Was ist die kleinste Baugruppe eines Salzes,also was ist damit gemeint?
Was ist ein Salzgitter?
2 Antworten

Moin,
ja, es liegt daran, dass Natriumchlorid eine Verbindung und kein Element ist.
Das Akronym HONClBrIF soll dich nur daran erinnern, dass die Elemente (!!) Wasserstoff (H), Sauerstoff (O), Stickstoff (N) sowie die vier Halogene Chlor (Cl), Brom (Br), Iod (I) und Fluor (F) nicht als kleinste Teilchen Atome, sondern zweiatomige Minimoleküle haben.
Wenn diese Elemente ohne anderen Bindungspartner in Reaktionsschemata (Reaktionsgleichungen) auftreten, dann sollst du daran denken, hinter das Elementsymbol eine tiefgestellte „2” als Index hinzuzufügen:
H2, N2, O2, F2, Cl2, Br2, I2
In Verbindungen können die Elementsymbole dagegen in allen möglichen Anzahlen vorkommen, zum Beispiel im Falle des Sauerstoffs... Da gibt es
- H2O (Wasser; 1 x O)
- CO2 (Kohlenstoffdioxid; 2 x O)
- CaCO3 (Calciumcarbonat, „Kalk”; 3 x O)
- KMnO4 (Kaliumpermanganat; 4 x O)
- V2O5 (Vanadiumpentoxid; 5 x O)
- C6H12O6 (Glucose, „Traubenzucker”; 6 x O)
- K2CrO7 (Kaliumdichromat; 7 x O)
- C8H18O8 (Octan-1,2,3,4,5,6,7,8-octol; 8 x O)
- C6H3N3O9 (Trinitrophloroglucinol; 9 x O)
- P4O10 (Phosphorpentoxid; 10 x O)
- ...
Es ist also ein großer Unterschied, ob du von den Elementen oder von Verbindungen sprichst...
Deine anderen Fragen gehören zu einem Komplex.
Salze sind aus Ionen aufgebaut. Ionen sind geladene Teilchen auf atomarem Größenniveau. Die Ladung kann positiv sein (dann spricht man auch von einem Kation) oder sie kann negativ sein (dann handelt es sich um ein Anion).
Die Ladung eines Ions wirkt nun aber nicht nur in eine, sondern in alle Raumrichtungen: Nach vorne, nach hinten, nach links, nach rechts, nach oben, nach unten, diagonal...
Entgegengesetzte Ladungen ziehen sich gegenseitig an (Plusladung zieht Minusladung an und umgekehrt). Gleichsinnige Ladungen stoßen sich dagegen voneinander ab (Plusladung stößt Plusladung ab, Minusladung stößt Minusladung ab).
Und nun stell dir folgendes vor: Im Verlauf einer chemischen Reaktion sind Milliarden und Abermilliarden von Natrium-Kationen bzw. Chlorid-Anionen entstanden.
Da die Ladung eines Natrium-Kations in alle Raumrichtungen wirkt, zieht es nun auch aus allen Raumrichtungen entgegengesetzt geladene Chlorid-Anionen an. Deshalb versammeln sich um das Natrium-Kation auch so viele Chlorid-Anionen, wie diese Platz finden.
Warum ist der Platz begrenzt? - Ganz einfach, der Platz ist begrenzt, weil sich irgendwann die gleichsinnig geladenen Chlorid-Anion, die sich um das Natrium-Kation ansammeln, irgendwann zu nahe kommen, je mehr von ihnen ankommen. Das heißt, dass sich die Chlorid-Anionen irgendwann anfangen, voneinander abzustoßen oder die Annäherung von weiteren Chlorid-Anionen zu gestatten.
So kommt es, dass um ein Natrium-Kation nicht mehr als sechs Chlorid-Anionen Platz finden. Eins links, eins rechts neben dem Natrium-Kation, eins darüber, eins darunter, eins davor und eins dahinter.
Nun ist es aber so, dass auch die Ladung der Chlorid-Anionen in alle Raumrichtungen wirken. Darum lagern sich nun auch um jedes der sechs Chlorid-Anionen so viele Natrium-Kation, wie jetzt diese Platz finden.
Und dann werden diese Natrium-Kationen ihrerseits wieder von so vielen Chlorid-Anionen umringt, wie Platz ist usw.
Du kannst nun sicherlich nachvollziehen, dass dadurch ein riesiges Ionengitter entsteht, in dem jedes Ion (egal ob Kation oder Anion) einen festen Platz einnimmt.
Dieses Ionengitter kann man auch als Salzgitter bezeichnen, weil ja - wie anfangs gesagt - ein Salz aus Ionen besteht (Ionengitter = Salzgitter).
Gleichzeitig entsteht mit dem Ionengitter aber auch eine hochgeordnete Struktur, da ja jedes Ion einen festen Platz einnimmt. Immer wenn es in der Chemie eine übergeordnete Struktur gibt, die hochgeordnet ist, bezeichnet man das als „krstallin”. Ein Ionengitter ist also Kristall. Ab einer bestimmten Menge an aneinandergelagerten Ionen kann man diese Kristalle sogar mit bloßem Auge sehen. Das passiert zum Beispiel, wenn du das Salz in einem Salzstreuer genauer betrachtest. Dann siehst du kleine Salzkristalle. Die gibt es auch in groß...
Wenn du verstanden hast, dass sich Ionen mit entgegengesetzt geladenen Ionen umgeben, verstehst du jetzt vielleicht auch, dass man in einem Ionengitter (einem Salzkristall) nicht mehr sagen kann, dass ein ganz bestimmtes Natrium-Kation mit einem ganz bestimmten Chlorid-Anion verbunden ist. Das Natrium-Kation hat ja insgesamt sechs Chlorid-Anionen, die es umgeben. Welches sollte man davon aussuchen? Das geht nicht.
Dennoch fällt auf, dass es stets gleich viele Natrium-Kationen wie Chlorid-Anionen in einem reinen Natriumchlorid-Kristall gibt.
Wenn also während der Reaktion zwischen Natrium und Chlor am Ende 2.554.337.201.004.598.234 Natrium-Kationen entstanden wären, dann hätte das auch zur Bildung von genau so vielen Chlorid-Anionen geführt.
Oder anders gesagt: Auf jedes Natrium-Kation in einem Salzkristall kommt ein Chlorid-Anion.
Deshalb ist es nicht sinnvoll, für eine Ionenverbindung wie ein Salz die genaue Anzahl der Ionen im Kristall anzugeben, sondern es ist zweckmäßiger, das kleinste Verhältnis der Ionen zueinander anzugeben.
Im Falle des Natriumchlorids wäre das daher: NaCl, weil auf jedes Natrium-Kation genau ein Chlorid-Anion kommt.
Aber diese sogenannte Verhältnisformel gibt natürlich keinen Aufschluss darüber, wie der Salzkristall tatsächlich aufgebaut ist.
Das gibt man mit der sogenannten Elementarzelle an:
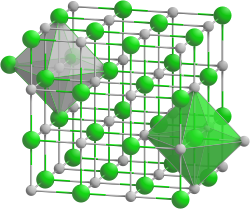
(grün: Chlorid-Anion; grau: Natrium-Kation)
Und da unterscheidet man Raumgruppen [in diesem Fall Fm3m (Nr. 225)], die Abstände zwischen den Ionen (hier a = 564,00 pm) und die Koordinationszahlen (im Falle des Natriumchlorids wäre das Na[6], Cl[6]).
Und dann können Fachleute der Kristallographie daraus ersehen, welche Form der Kristall hat (bei Natriumchlorid ist das ein kubischer Kristall, der im Grunde würfelförmig ist).
Aber ich bezweifle, dass du das so genau wissen musst; zumindest nicht, wenn es um Schulchemie geht, worauf deine Fragen schließen lassen...
Ich hoffe, die Zusammenhänge sind dir nun ein bisschen klarer geworden.
LG von der Waterkant
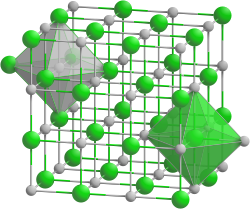

NaCl
Na=Metall
Cl=Nichtmetall
Bei einer Metall-Nichtmetall Verbindung ist es eine Verhältnisformel.
Du hast Recht, Cl steht im HONClBrIF.Das heißt das reines Cl aus Molekülen( die aus he 2 Atomen bestehen) besteht.


Ja aber warum muss man dann einige Verhältnisformel noch ausgleichen oder so?

Du meinst bei einer Gleichung?
1Na+1Cl=1NaCl ?
Die 1 kannst du auch weglassen.
Erklärung:
Auf beiden Seiten des Gleichheitszeichens muss die gleiche Anzahl sein.
Links vom Gleichheitszeichen ist 1 Na und 1 Cl.Rechts vom Gleichheitszeichen ist auch 1 Na und 1 Cl.