Titration von Citronensäure?
Hallo,
warum wird bei der Titration von Citronensäure 1M NaOH und nicht 0,1M NaOH als Maßlösung verwendet?
Danke
1 Antwort
Man wählt die Konzentration der Maßlösung so, daß man bei der Titration einen vernünftigen Verbrauch (mehr als 10 ml, weniger als 100 ml) hat. Andererseits kann man ja die Stoffmenge im Kolben durch Aliquotierung ziemlich beliebig gestalten; meist macht man es so, daß man mit 0.1 mol/l NaOH auskommt (die greift Glas nicht so stark an wie 1 mol/l). Wenn eine Titration zu stark von der Stärke der Maßlösung abhängt, dann sollte man sich sowieso Alternativen überlegen.
Bei der Zitrone ist es übrigens weitgehend egal, mit welche Maßlösung Du titrierst. Zum Beweis füge ich Titrationskurven von 20 ml Zitronensäure (1, 0.1 und 0.01 mol/l) mit gleich starker NaOH an. Der Äquivalenzpunkt bei 60 ml Verbrauch ist in jedem Fall sehr gut sichtbar. Die Hintergrundfarben geben die Speziesverteilung (freie Säure rot, Dihydrodrogencitrat rotviolett, Hydrogencitrat blauviolett und Citrat blau) an; die Speziesverteilung ist schon konzentrationsabhängig, aber das schlägt nur wenig auf die Titrationskurve zurück: Der Sprung wird zwar jeweils um ca. eine pH-Einhet kleiner, bleibt aber immer noch im gut detektierbaren Bereich.





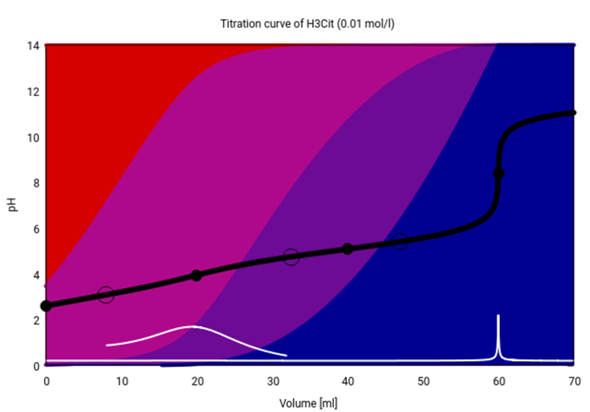
Wieviel Zitronensäure hast Du denn in Kolben? Oder was ist sonst als Randbedingung gegeben? Als generelle Aussage „H₃Cit soll immer mit 1 mol/l NaOH titriert werden“ wäre es falsch, wie die Titrationskurven belegen. Jeder Sprung von drei oder mehr pH-Einheiten ist gut genug für eine Titration.
das ist die Frage:
Sie wollen Zitronensäure (192 g/mol) bestimmen, haben aber ihre Substanz ausversehen in HCl gelöst. Um keine A-Analyse zu kassieren, bestimmen Sie mit 1 M NaOH.
Warum verwendet man zur Bestimmung der Zitronensäure nach Ph. Eur. eine 1 M NaOH und nicht wie üblich eine 0,1 M NaOH. Begründung mit Rechnung!
- Wenn ich weiß, wieviel HCl ich dazugegegeben habe, dann kann ich ja trotzdem titrieren und muß nur von meinem gemessenen Verbrauch das abziehen, was von der HCl neutralisiert wurde. Wenn ich die Stoffmenge der versehentlich zugesetzten HCl nicht kenne, habe ich ein dickes Problem (mit Phosphorsäure ginge es immer noch, weißt Du auch wie?)
- Das dürfte wohl im Detail an der Vorschrift in Ph Eur liegen (aber ich kenne sie nicht). Es wäre auch denkbar, daß das wegen irgendwelcher erwarteten Verunreinigungen gemacht wird, um deren Störung niedrig zu halten. Oder eben for hysterical raisins.
War eine Klausur Aufgabe und ich muss es rechnerisch beweisen wieso die Anwendungen von 1M NaOH besser ist