Redoxgleichungg?
Stellen Sie die Reaktionsgleichungen richtig auf. Was wird oxidiert, was wird reduziert?
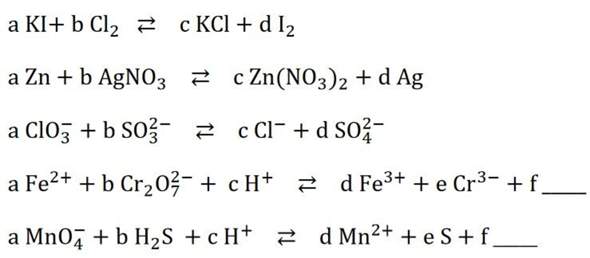
2KI + Cl2 ⇄ 2KCl + I2
I wird oxidiert, Cl wird reduziert
Zn + AgNO3 -> Zn(NO3)2 + Ag
Ag wird reduziert, Zn wird oxidiert
2(ClO3)- + 3(SO3)2- --> 2Cl- + 3(SO4)2-
wird nix oxidiert und reduziert
6Fe2+ + Cr2O72− + 14 H+ --> 6 Fe3+ + 2 Cr3+ + 7H2O
Fe wird oxidiert, Cr wird reduziert
2MnO4- + 5H2S + 6H+ --> 2Mn2+ + 5S + 8H2O
Mn wird reduziert, S wird oxidiert
richtig?
1 Antwort
Das die "Gleichungen" noch nicht ausgeglichen sind, ist dir klar?
Ansonsten hast du die oxidierten/reduzierten Elemente richtig identifiziert, bis auf auf Aufgabe drei.
Da wird Chlor von OZ +5 (Chlorat) zu OZ -1 (Chlorid) reduziert, während Schwefel von +4 (Sulfit) zu +6 (Sulfat) oxidiert wird.
Deshalb ist das Mengenverhältnis hier auch 1:3 und nicht 2:3.
Zn + 2AgNO3 -> Zn(NO3)2 + 2Ag
die restlichen Gleichungen alle richtig?