Molekül N3?
Normalerweise gibt es ja n als n2 Molekül sowie O als O2 Molekül aber gibt es ein N3 Molekül ?
Mit Begründung bitte danke
2 Antworten
Das N₃ hat eine ungerade Elektronenanzahl und ist daher extrem instabil; es wurde experimentell nachgewiesen, in einer Matrix aus festem Edelgas bei nur wenigen Grad über dem absoluten Nullpunkt. Fapp existiert es nicht. Wenn man weiß, daß bereits HN₃ (mit gerader Elektronenanzahl) beim Hinsehen explodiert, wundert man sich auch nicht darüber.
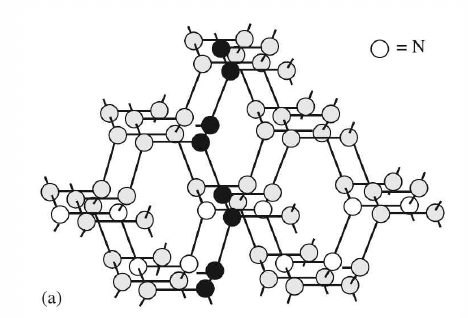
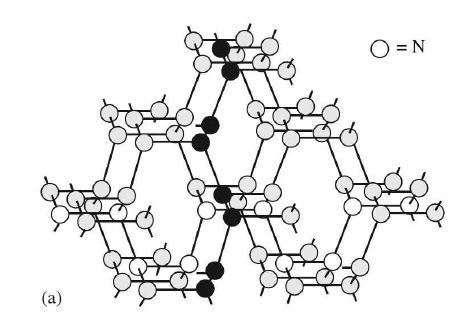
Es gibt allerdings N₄ (tetraedrisch wie P₄ als Singulett mit allen Elektronen gepaart, etwas stabiler kettenförmig als Triplett mit zwei ungepaarten Elektronen), und das ist extrem kurzlebig (in verdünntem Gas im Massenspektrometer Mikrosekunden). Etwas ziviler verhält sich polymerer Stickstoff, der bei hoher Temperatur (2000 K) und extremem Druck (1 Mbar) hergestellt werden konnte, aber sich auch nicht wirklich zum Hausgebrauch eignet. Die Struktur ist ähnlich wie im Diamant, also jedes N-Atom ist in einem 3D-Gitter kovalent an seine drei Nachbarn gebunden, mit „Löchern“ dort, wo beim Diamanten der vierte Bindungspartner wäre.