Kann jemand diese Chemie-Aufgabe lösen?
Ich bin im Studium und habe eine Chemie-Aufgabe bekommen, die ich bis heute Abend abgeben muss. Für die richtige Antwort kriege ich Punkte, die mir dann bei der Prüfung dazugerechnet werden. Leider ist mein Vorwissen von der Oberstufe nicht so gut, deswegen verstehe ich die Aufgabe nicht ganz und habe bis heute Abend nicht genug Zeit, das im Detail durchzugehen, um es zu verstehen.
Also kann mir jemand helfen und diese Aufgabe lösen bzw. mir auch erklären??
Thema: Räumliche Struktur nach dem EPA-Modell
Phosphorige Säure und Phosphonsäure stehen in einem Tautomerie-Gleichgewicht. Haben die Anionen Phosphit und Phosphonat die gleiche räumliche Struktur? Wenn ja, welche räumliche Situation liegt am Zentralatom vor? Falls das nicht der Fall sein sollte, dann geben Sie die räumliche Struktur für beide Anionen an. Ergänzen Sie Ihre Antwort um eine kurze Begründung, wie Sie auf die angegebene räumliche Struktur kommen.
Das würde mir echt viel helfen & danke im Voraus! :)
2 Antworten
Wenn Du mit räumlicher Struktur die "Realstruktur" meinst, sind die Strukturen natürlich unterschiedlich.
Nach den EPA (oder VSEPR)-Regeln sind die Pseudostrukturen (also wo auch das freie Elektronenpaar der Phosphorigen Säure als Ligand gilt) bei beiden tetraedrisch (4 Liganden; Zentralatom in der Mitte des Tetraeders).
Für die Realstruktur wird das freie Elektronenpaar nicht mehr betrachtet und übrig bleibt eine trigonal-pyramidale- Struktur für die Phosphorige Säure (Zentralatom als Spitze einer trigonalen Pyramide).
Phosporige Säure/ Phosphan ist eine zweiwertige Säure und damit können nur die Protonen aus der OH Gruppe abgegeben werden. D.h. das die Anionenstrukturen dieselben sein müssten wie die Struktur der Säuren.
Allerdings denke ich nicht das eine tautomere Form für Salze besteht, sondern das eher nur die Phosphanvariante als Anion für Salz stabil ist.

Die freie Säure und die einfachen Salze enthalten trigonal pyramidale bzw. tetraedrische Anionen mit einem unmittelbar an den Phosphor gebundenen Wasserstoffatom. Wobei das freie Elektronenpaar räumlich mehr Platz beansprucht und somit die trigonale Pyramide verzerrt (platter macht).
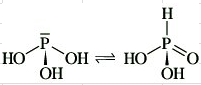
okay danke! und was ist die Strukturformel der beiden Anionen?