Formelgleichung (Chemie) erstellen?
Ich schreibe morgen eine Chemie Schulaufgabe und unter anderem über das erstellen von Formelgleichungen.
Ich habe hier 2 Aufgaben wo ich am verzweifeln bin. Siehe Arbeitsblatt :
Ich soll die formelgleichung richtig stellen. Ich benötige Hilfe! Bitte auch mit Lösungsweg!
Vielen Dank! :)
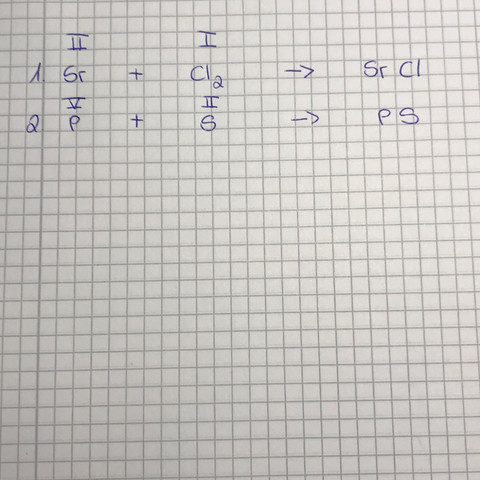
4 Antworten
Chlor wird in der Reaktion definitiv Elektronen aufnehmen (Achtung geht auch anders rum zB mit Sauerstoff) Das solltet du auch raufschreiben -I. Strontium, ein Erdalkalimetall wird 2 Elektronen (immer) abgeben, also +II. Wie viele Chloratome müssen also mit Strontium reagieren damit Strontiumchlorid, ungeladen, rauskommt? Das schreibst hinten mal an die Reaktionsprodukte. so wie in diesem Beispiel:
Cl + O --> Cl2O7 (diverse Zwischenreaktionen, direkt geht's nicht) wenn Cl + VII reagiert und O - II (Chlor hat auch andere Reaktionsstufen.) Nun ist diese Gleichung nicht fertig. Chlor kommt in der Natur nur als 2-Atomiges Molekül, Cl2 vor. Sauerstoff kommt als O2 vor (O3 wird Ozon genannt).
Also Cl2 + O2 --> Cl2O7
Nun müssen rechts und links die Stoffmengen passen, ergo etwas Mathematik (Stöchiometrie).
2Cl2 + 7O2 --> 2Cl2O7.
Kleiner Tipp: Schwefel reagiert mit Phosphor auch -II.
Hi,
ist gar nicht soooo schwer:
Wenn du dir eine Tüte Chlor kaufst und reinschaust, dann siehst du, daß da immer zwei zusammenkleben. Chlor und einige andere Chemikalien (z.B. H2, O2. N2, F2, Br2) gibt es sozusagen nur als "Bundle". Diese Genannten musst du dir tatsächlich mal als "Doppel" merken. Wenn du diese in einer Gleichung hast, musst (!) du immer Cl2 schreiben. Nicht: 2 Cl
Jetzt schaust du auf die 8 Hauptgruppen im PSE: Alle Elemente wollen entweder "Null" oder "8" erreichen (=Oktettregel)
Sr steht in der 2. Hauptgruppe, könnte also 6 Elektronen aufnehmen oder viel einfacher: 2 abgeben ("Null"). deswegen die 2 darüber.
Ebenso Chlor. Steht in der 7. Hauptgruppe, köönte also 7 Elektronen abgeben oder viel einfacher: Eines aufnehmen ("Acht")
Ein Sr gibt also 2 Elektronen ab, ein Chlor kann nur eines aufnehmen. Daher brauchst du 2 Chlor. Die Formel für das entstehende Produkt heißt also SrCl2
Praktischerweise kommt Chlor sowieso nur als Bundle vor: Ein Sr reagiert also mit einem "Bundle"-Chlor zu dem vorher gefundenen Produkt:
Sr + Cl2 -> SrCl2
m.f.G.
anwesende
Hallo Celinemattess
die Oxidationszahlen (OZ) in den Edukten sollen wohl die OZ in den Produkten werden.
Gleichung 1
Sr + Cl2 ==> SrCl2
Strontium wird von 0 auf +2 oxidiert, jedes Chlor von 0 auf -1 reduziert
Gleichung 2
4 P + 10 S ==> P4S10
formal würde auch P2S5 gehen, aber das Molekül liegt - wie P2O5/P4O10 - als Dimeres vor
Phosphor wird von 0 auf +5 oxidiert, Schwefel von 0 auf -2 reduziert.
LG
Sr + Cl₂ ⟶ SrCl₂
8 P₄ + 10 S₈ ⟶ 8 P₄S₁₀
Wär halt schön wenn der Chemie ich hab kein Bock, auch etwas lernen im Sinne von verstehen würde, nicht nur Abschreib- und Auswendiglernübung...