Wie kann man erklären,dass Alkohol und Wasser durch Destillation voneinander getrennt werden können und was nutzt man dazu?
3 Antworten
Gehen wir man von Wasser und Ethanol aus (ich kenne es so das Alkohol meistens Ethanol heißt) dann hat Wasser einen höheren Siedepunkt als Ethanol. Der von Wasser liegt bei ca. 100 °C der von C2H5OH bei ca. 78°C. Dadurch verdampft Ethanol "früher" also bei geringerer Temperatur. Man erhitzt das Gemisch auf die 78 °C, sodass das Ethanol verdampft. Da Wasser dabei noch nicht siedet , lediglich etwas verdunstet kann man das Ethanol gut vom Wasser trennen. Durch mehrfache Destillation kann man die Konzentration vom Ethanol erhöhen.
Zusammengefasst:
1. Durch die unterschiedlichen Siedepunkte, kann man Ethanol und Wasser trennen, indem man das Gemisch auf den niedrigeren Siedepunkt erwärmt, indem Fall Ethanol.
2. Die unterschiedlichen Siedepunkte/Siedetemperaturen
Alkohol hat einen niedrigeren Siedepunkt. Wenn man das Wasser-Alk-Gemisch auf eine bestimmte Temperatur erhöht, wird nur der Alkohol gasförmig und lässt sich auffangen
Alkohol (also ich gehe hier mal vom Stoff Methanol aus) hat einen geringeren Siedepunkt als Wasser. Das Alkohol-Wasser Gemisch wird also auf den Siedepunkt des Alkohols erhitzt. Dieser wird dann gasförmig, steigt auf und wird dann aufgefangen. Nun wird er wieder abgekühlt und somit wieder flüssig gemacht. Nach der Destillation hat man das Wasser vom Alkohol getrennt.
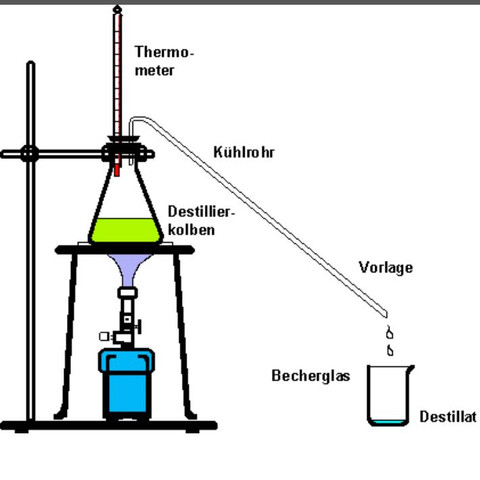
Ich füge nochmal ein Foto ein.
Hoffe ich konnte helfen