Wie viel Arbeit muss verrichtet werden (c)?
Hiiii, ich schon wieder, am selben Tag.
Dieses Mal geht um Aufgabe c.
Mein Kopf will heute scheinbar nicht mehr, also bitte hilfe!

Danke im Voraus!
Das hier sind die Musterlösungen,

Und das ist eine Formel, die ich gefunden habe, welche mir so scheint, als könnte sie helfen, aber sie funktioniert bei mir irgendwie nicht!

2 Antworten
Wie lautet denn die musterlösung? Entweder steh ich auf dem Schlauch oder das ist echt so komisch gestellt, aber in meinem Verständnis ist die Arbeit, die an der kolbrnstange verrichtet wird gleich die volumenänderungsarbeit aus b)
Edit:
Nutzarbeit der kolbenstange, umgebungsdruck muss beachtet werden:
W_nutz = W_v + p_amb (V2-V1)
= - 1546,7 J + 100.000 Pa * (0,05-0,025) m^3
= 953,3 J
Okay die antwort scheint richtig zu sein und irgendwie sinn zu ergeben, aber das ganze ist schon irgendwie sehr komisch. Aber definitiv danke!!!
Hab meine Antwort bearbeitet. Stand echt auf dem Schlauch aber die Aufgabe ist auch blöd gestellt.
Und das ist eine Formel, die ich gefunden habe,
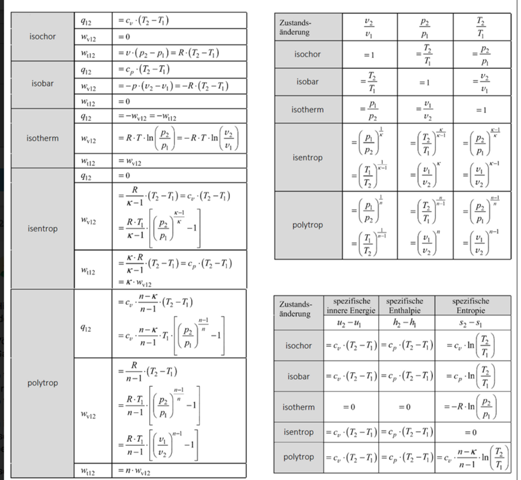
Die ist in der Tat eher suboptimal. Hier ist eine schöne Übersicht über alle polytropen Zustandsänderungen idealer Gase incl. der diversen Sonderfälle:

a) Nun suchen wir uns die Formel raus, die den Zusammenhang zwischen Volumen, Temperatur und Polytrope herstellt:

v2/v1 = V2/V1, da die Masse konstant bleibt. Das lösen wir nach n auf:

b) Nun suchen wir uns die Formel für die Volumenänderungsarbeit bei einer polytropen Zustandsänderung heraus, setzen die Werte ein und rechnen:

Da kriegen wir aber nur die molare Volumenänderungsarbeit raus. Wir suchen aber den absoluten Betrag, also müssen wir die Mole Luft im Zylinder ausrechnen. Vorsicht: n ist das Formelzeichen sowohl für die Zahl Mole als auch für den Polytropenexponent. Das muss man auseinanderhalten:

Nun können wir den Absolutbetrag der Volumenänderungsarbeit ausrechnen:

Die Differenz in der letzten Ziffer dürfte Rundungsfehlern geschuldet sein.
Diese Arbeit könnten wir an der Kolbenstange aber nur dann abnehmen, wenn sich der Zylinder im Vakuum befnden würde. Dann würde der Kolben tatsächlich durch die Entspannung im Zylinder Arbeit abgeben, daher das negative Vorzeichen. Durch die abgegebene Arbeit verringert sich gemäß 1. Hauptsatz die innere Energie, was sich in der Temperaturabsenkung bemerkbar macht.
c) Nun ist es aber so, dass durch die Bewegung des Kolbens die Luft in der Umgebung sozusagen komprimiert wird oder anders gesagt, es muss Arbeit gegen den Umgebungsluftdruck verrichtet werden. Durch die Kolbenbewegung dürfte sich der Luftdruck der Umgebung nicht ändern, weshalb wir die passende Formel bei "isobar" suchen müssen:

Dabei haben wir statt v wieder V verwendet.
Nun können wir die Gesamtarbeit, genannt technische Arbeit Wt, berechnen, die an der Kolbenstange verrichtet werden muss bzw. abgenommen werden kann:

Das positive Vorzeichen sagt uns, dass diese Arbeit dem Gesamtsystem zugeführt wird. Wir müssen also kräftig an der Kolbenstange ziehen.
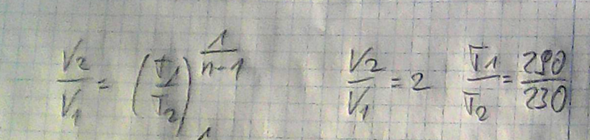
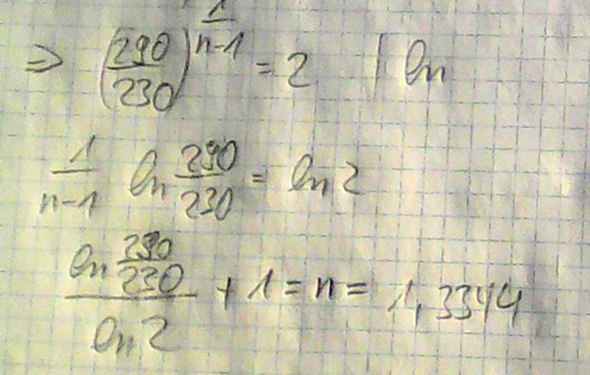
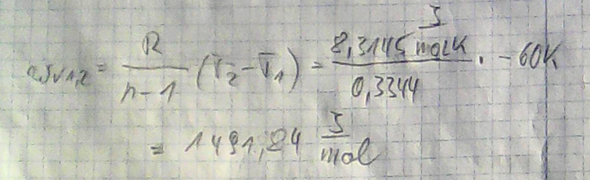
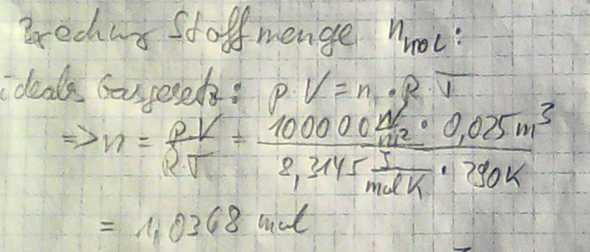
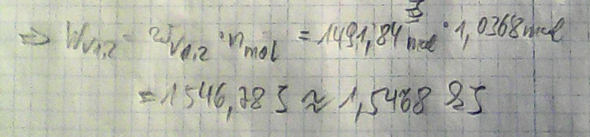
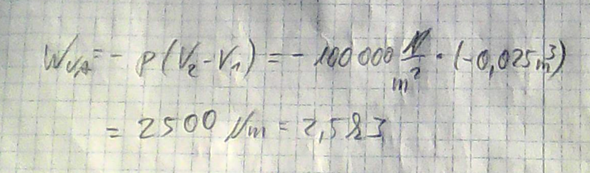
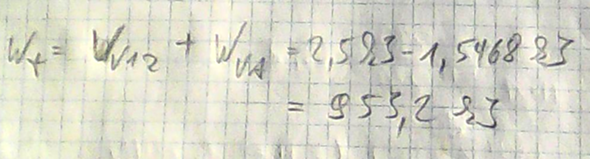
Ich habe die Musterlösungen hinzugefügt.