Wie stellt man Natriumacetat her?
Also ich weiß, dass man dafür Natron & Essigessenz brauch. Aber welche Menge? Und jetzt bitte keine Antworten wie es muss nur neutral sein, ich bin in Chemie echt schlecht & brauche mengenangaben in Gramm oder Milliliter bitte. :) Danke schonmal :3
3 Antworten
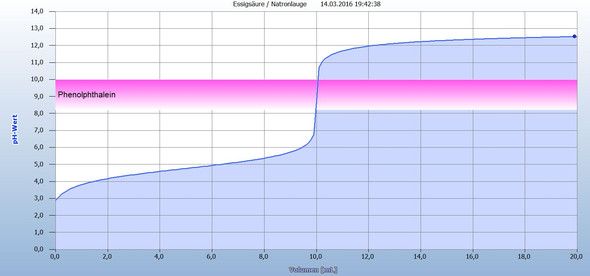
Ich habe Dir folgenden Versuch als Graphik in der Anlage beigegeben:
Man legt Essigsäure (V = 10 mL, c = 0,1 mol/L) vor und titriert mit Natronlauge (V = 20 mL, c = 0,1 mL).
Du ersiehst aus der Grafik, dass der Äquivalenzpunkt nach Zugabe von V(Natronlauge) = 10 mL erreicht ist. Mit dem Indikator Phenolphthalein würde man das Erreichen des Äquivalenzpunktes erkennen.
Würde man hier die Titration abbrechen und die Lösung "zur Trockne" eindampfen, dann würde Natriumacetat auskristallisieren.
Du siehst aus dem pH am Äquivalenzpunkt, dass pH ≠ 7.
Der Neutralpunkt ≠ Äquivalenzpunkt bei dieser Titration.
- Reaktionsgleichung aufstellen
- Molmassen berechnen
- Einsatzmengen berechnen
- Versuch durchführen
1. NaHCO3 + CH3COOH ———> CH3COONa + H2O + CO2
2. 84,01 g/mol + 60,05 g/mol -> 82,03 g/mol
3. Der Einfachheit halber nehmen wir an, dass Du 84g Küchennatron in der Apotheke kaufst und genau 25%ige Essigessenz zur Verfügung hast. Du brauchst also ein mol Essigsäure = 60g = 240g 25% Essenz
4. Leg die 240g Essigessenz vor und gib das Natron unter Rühren langsam dazu; wenn die Schaumbildung aufgehört hat beginne die Lösung langsam zu erhitzen und dampfe sie ein. Zuerst werden weiße Kristalle ausfallen, wenn alle Flüssigkeit verdampft ist, bleiben nur weiße Kristalle übrig. Dabei handelt es sich um das Na-Acetat-Trihydrat. Das muss jetzt eine Zeit auf über 120°C erhitzt werden um das Kristallwasser auszutreiben. Übrig bleiben 82g wasserfreies Natriumacetat. (Muss unter dichtem Verschluss aufgehoben werden, da stark hygroskopisch).
Man sollte nichts herstellen, von dem man nicht versteht, wie man es herstellt.
MIT MENGENANGABEN!
Wäre so, als würdest du etwas kaufen, und willst die Anzahl Scheine/Münzen wissen, aber ja nicht so Kleinigkeiten wie den aufgedrückten/eingeprägten Wert.
Ich gebe auch Nachhilfe, für 42.