Warum sind die Van-der-Waals-Kräfte bei der Trans-Konfiguration schwächer?
2 Antworten
Ich mache ein paar Annahmen über Deine Frage, so daß sie beantwortbar wird.
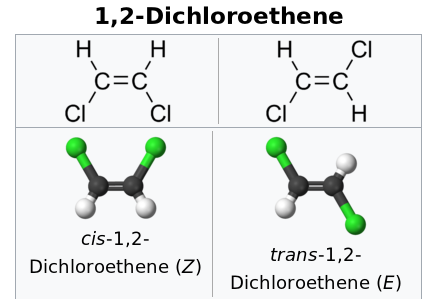
Alkene und ähnliches Zeug kommen mitunter in zwei Isomeren vor. Ein Beispiel wäre das 1,2-Dichlorethen CHCl=CHCl, da gibt es eine trans-Form (in saubererer Terminologie: E) und eine cis-Form (besser: Z). Das E-Isomer schmilzt bei −50 °C und siedet bei 49 °C, beim Z-Isomer sind die beiden Phasenübergangstemperaturen −81 und 60 °C.
Die beiden Isomere entalten dieselben Bindungen, und sollten daher auch ungefähr gleichartige intermolekulare Wechselwirkungen zeigen. Gemeinhin nimmt man an, daß Schmelz- und Siedepunkt von der Stärke genau dieser Kräfte bestimmt werden. Aber warum gibt es überhaupt einen Unterschied zwischen den beiden, und warum schmilzt das Z-Isomer höher aber siedet tiefer?
Der Grund liegt in der Symmetrie: Wenn wir berücksichtigen, daß Chlor viel größer ist als Wasserstoff, dann sieht das Z-Isomer wie eine Sichel aus (oder wie der Buchstabe C), das Z-Isomer aber wie ein S:
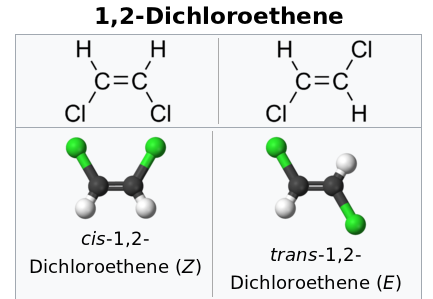
Und das hat drastische Folgen: Das E-Isomer hat Dipolmoment Null, weil sich die einzelnen Bindungsdipole genau kompensieren; damit erklärt sich warum die Moleküle einander weniger anziehen und der Siedepunkt tiefer liegt. Dagegen hat das Z-Isomer ein Dipolmoment etwa so groß wie Wasser, und daher ziehen einander die Moleküle stärker an, und es braucht mehr Energie, sie zu trennen. Daher hat das Ding einen höheren Siedepunkt.
Andererseits lassen sich die E-Moleküle offenbar viel besser zu einem Kristall zusammenfügen als die Z-Moleküle. Beim Kristallisieren kommt es auch auf die vdW-Kräfte an, aber die Molekülform spielt auch eine Rolle, weil manche Formen sich leichter und enger zu einer 3D-Struktur zusammenfügen lassen. Hier gewinnt die E-Form, weil zwar die Kräfte geringer sind, aber die Moleküle besser gepackt werden können (da sie alle diese S-Form haben, schmiegen sie sich besser aneinander).
Was verstehst du unter Trans-Konfiguration?