Konzentrationen bestimmen?
Eine Verbindung besteht aus aus Zn^2+, K^+ und Cl^ - ionen
c(K+)= 0,2 mol/l und c(Cl-) = 0,8 mol/l
Wie groß ist die Zinkionenkonzentration?
Und wie berechnet man diese?
1 Antwort
Die Ausgangsannahme ist, dass die Konzentration der Kalium-, Zink- und Chloridionen anfänglich 0 mol/l beträgt.
Nach der Zugabe der Salze, also Zink(II)-chlorid und Kaliumchlorid beträgt die Konzentration der Chloridionen 0.8 mol/l, während die Konzentration der Kaliumionen 0.2 mol/l entspricht.
Da im Salz Kaliumchlorid das Verhältnis von Chlorid- zu Kaliumionen 1:1 entspricht, ist die Stoffmenge und somit auch die Konzentration der Chloridionen identisch mit der der vorliegenden Kaliumionen.
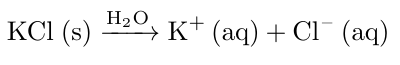
Folglich gilt:
Die tatsächlich vorliegende Konzentration der Chloridionen ist jedoch größer. Diese Konzentrationsdifferenz kommt durch die Chloridionen des Zink(II)-chlorids zustande.
Da das Verhältnis von Zinkionen zu Chlorionen im Salz Zink(II)-chlorid 2:1 beträgt, bedeutet dies, dass die Stoffmenge und somit die Konzentration der Zinkionen halb so groß ist, wie die Konzentration der Chloridionenkonzentrationsdifferenz.
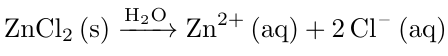
Folglich beträgt die Konzentration der Zinkionen 0.3 mol/l.
~Johannes
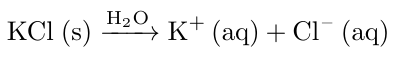
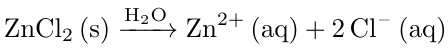
Vielen vielen Dank !! Das hat mir sehr weitergeholfen! :)