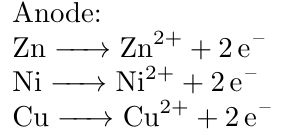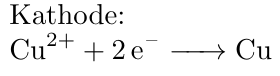Hilfe bei dieser Chemie-Aufgabe?
Wie man die Masse berechnet. weiß ich. Aber kann mir jemand bitte die obere Aufgabe erklären.
1 Antwort
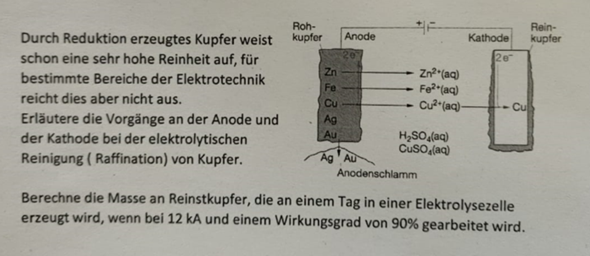
Der vorliegende Prozess ist die elektrolytische Kupferraffination, die bei einer äußerst geringen Spannung von circa 0.3V durchgeführt wird. Durch die angelegte Spannung soll die Ausbeute an Kupfer erhöht werden. Jedoch darf diese Spannung nicht zu hoch ausfallen, da andernfalls auch andere unerwünschte Stoffe reduziert werden und so zu einer Verunreinigung des entstehenden Kupfers führen würden.
An der Kupferanode kommt es zur Oxidation der Kupferatome und der Metall-Atome der Elemente, die unendler sind als Kupfer. Hierzu gehören beispielsweise Zink, Eisen und Nickel.
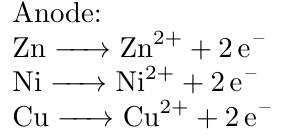
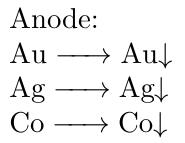
Metall-Atome der Elemente, die edler sind als Kupfer fallen als Anodenschlamm ab. Dazu gehören beispielsweise Gold, Silber und Kobalt.
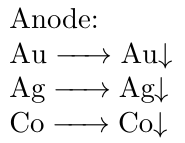
An der Kathode, an welcher der Minuspol anliegt, kommt es zur Reduktion von Kupfer(II)-Kationen zu Kupferatomen. Dabei bildet sich an der Kathode nahezu reines Kupfer.
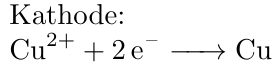
Durch die niedrige Spannung bei der Kupferraffination wird auch die Reduktion von Kationen unreinerer Stoffe als Kupfer größtenteils unterbunden.
~JackboyPlay