Einfachbindung, Doppelbindung, Dreifachbindung?
Ich würde gerne wissen, ob man bei einer Einfachbindung sagen kann, dass es eine Atombindung mit einem bindenden Elektronenpaar ist, bei einer Doppelbindung, dass es eine Atombindung mit zwei bindenden Elektronenpaaren ist und bei einer Dreifachbindung, dass es eine Atombindung mit drei bindenden Elektronenpaaren ist. Meine Frage bezieht sich auf die Formulierung „eine Atombindung“, da ich mir nicht sicher bin, ob man dann bei der Doppelbindung „zwei Atombindungen“ und bei der Dreifachbindung „drei Atombindungen“ sagt.
Bei der Einfachbindung kann ich es so schreiben, oder?
1 Antwort
Die verschiedenen Bindungsarten ergeben sich aus der elektronischen Struktur der Bindungspartner. Bei einer Einfachbindung liegt eine sogenannte Sigmabindung vor.
Stell dir das Wasserstoffmolekül vor. Bei einem einzelnen Wasserstoffatom ist die Aufenthaltswahrscheinlichkeit des Elektrons in allen Richtungen um den Atomkern überall gleich groß und nimmt lediglich mit wachsendem Abstand zum Kern ab. Du kannst dir diesen Aufenthaltsort wie eine Sphäre um den Atomkern vorstellen. Bei einem Wasserstoffmolekül überlappen nun diese Sphären. Die Bindungsachse ist daher rotationssymmetrisch. Diesen Bindungstypus bezeichnet man als Sigmabindung.
Energetisch höher liegende Elektronen halten sich unter Umständen nicht mehr gleichmäßig wahrscheinlich um einen Atomkern auf. Es gibt neben den sphärischen Aufenthaltsorten (s-Orbitale) auch die sogenannten p-Orbitale. p-Orbitale können natürlich auch überlappen. Dann spricht man von einer Pi-Bindung (Pi, wie das Symbol der mathematischen Kreiszahl). Eine Pi-Bindung ist achsensymmetrisch aber nicht rotationssymmetrisch. Bei einer Doppelbindung liegt neben einer Sigmabindung auch eine Pi-Bindung vor. Bei einer Dreifachbindung liegen eine Sigma-Bindung und zwei Pi-Bindungen vor.
Wenn du sagst, dass bei einer Doppelbindung "drei Atombindungen" vorlägen musst du das konkretisieren. Die zwei Bindungen in einer Doppelbindung sind nicht gleichartig. Einmal hast du eine Sigma- und einmal eine Pi-Bindung.
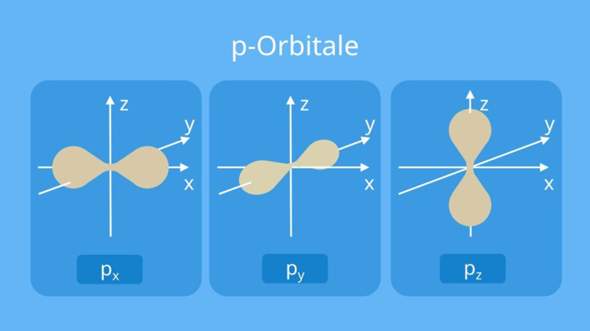
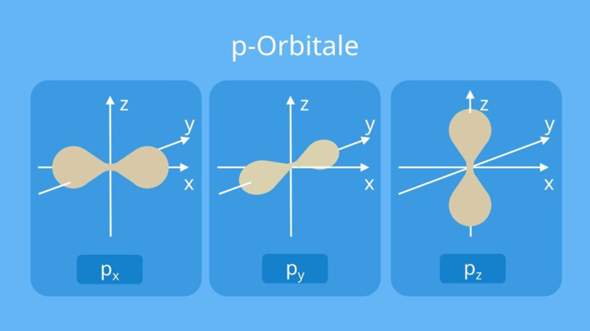
Auch p-orbitale können zu einer Sigma Bindung überlappen, wenn sie "aufeinander zu" zeigen
Ein bindendes Elektronenpaar liegt bei jeder kovalenten Bindung vor. In einer Einfachbindung steckt ein bindendes Elektronenpaar; in einer Doppelbindung stecken zwei bindende Elektronenpaare.
Ich meine eigentlich, dass ich gerne wissen würde, ob man eine Einfachbindung, eine Doppelbindung etc. allgemein als Begriff als „eine Atombindung“ betitelt oder ob man auf die Anzahl an bindenden Elektronenpaaren eingeht und dann stattdessen die Anzahl an Atombindungen sagt. Dann würde angenommen eine Doppelbindung zwei Atombindung haben.
Stell dir eine Bindung wie eine Kette vor. Bei einer Einfachbindung sind zwei Kugeln mit einer Kette verbunden, bei einer Doppelbindung mit zwei Ketten.
Hat eine Doppelbindung zwei Atombindungen mit zwei bindenden Elektronenpaaren oder eine Atombindung mit zwei bindenden Elektronenpaaren?