Zinksulfid als Teilchenmodell?
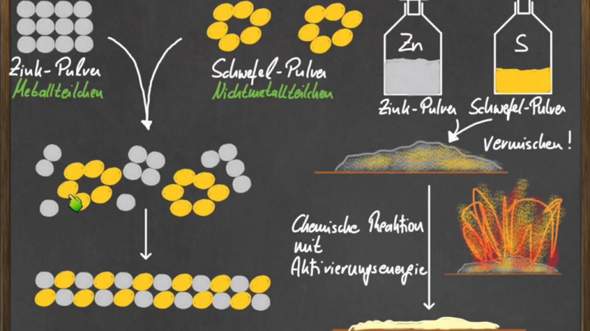
ich brauch in Chemie ein Teilchenmodell von Zinksulfid ich hab gegoogelt und ist das so richtig ?
1 Antwort
hmm, naja, prinzipiell schon...
Da hat sich jemand richtig viel Mühe gegeben und dann (wenn auch unwichtigen) Quatsch falsch gemacht.
Schwefel bildet tatsächliche Ringe, aber es sind 8er Ringe und normalerweise keine 6er! (eigentlich ist das aber unwichtig).
Das Zinksulfid sieht aus wie eine dünne Schicht und man erkennt das Muster kaum! Ich würde eher ein Rechteck, oder Quadrat mit so einem SchachbrettMuster zeichnen, damit es deutlicher wird!
Stimmt zwar, aber 1. gibts den nur in einem kleinen TemperaturBereich.
und 2. ist das AnfangsUnterricht, wo das irrelevant ist.
Entweder man lässt es ganz weg (wie kurz danach auch in Reaktionsgleichungen), oder man verwendet 8er Ringe.
Naja, λ-Schwefel kommt vorwiegend in den Ringgrößen 6,7,9,12 bis 26 vor, also ist jetzt Auslegungssache, aber nur S8 gibt ea definitiv nicht.