Wie ist bestimmt man die Oxidations bei folgender Gleichung?
Wie bestimmt man die OZ bei dieser Gleichung?
Bitte nicht darauf achten was ich bereits in rot hingeschrieben hab. Wäre sehr dankbar wenn mir jemand helfen könnte!
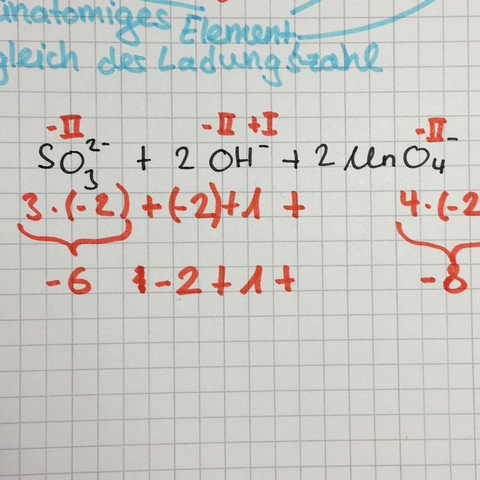
2 Antworten
"Die Summe der Oxidationszahlen ist identisch mit der Ladung des Moleküls". (<= Merken! Gilt immer und überall.)
____________________________________________________________
Für dein Sulfit (SO3[2-]) gilt damit:
S + O + O + O = 2-
Da du weißt, dass "O = -II", kannnst du einsetzen:
S + (-II) + (-II) + (-II) = 2-
Also muss S die OZ + IV bekommen, damit die Rechnung stimmt.
____________________________________________________________
Für dein Permangant (MnO4[-]) gilt damit:
Mn + O + O + O + O = -1
Und nun probier mal, die OZ von Mn zu bestimmen...
____________________________________________________________
LG
MCX
Bei SO3 musst du auf -2 kommen, also
X + 3*(-2)= -2 demzufolge muss die Oxidationszahl von S = 4 sein