Wie hat mein Chemielehrer diese blaugeschriebenen Sachen herausgefunden?
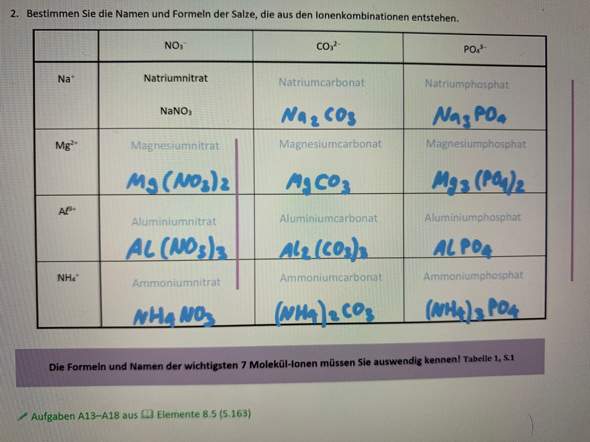
Ich verstehe es wenn zb „Aluminiumoxid“ gegeben ist, muss man im Periodensystem schauen und findet heraus, dass die Formel „Al2O3“ ist. Jedoch verstehe ich die untere Aufgabe nicht. Kann mir jemand helfen? Wäre sehr dankbar:)
Und was bedeutet diese Klammer?
2 Antworten

Die Formeln der Ionen stehen in der Tabelle. Man muss die jeweilige Anzahl so kombinieren, dass sich positive und negative Ladungen ausgleichen.
Alu bildet Al(3+)-Ionen (Metall der 3. Hauptgruppe) und Sauerstoff O(2-)-Ionen (Nichtmetall der 6. Hauptgruppe).
Das kleinste gemeinsame Vielfache ist 6. Also benötigt man 2× Al(3+) und 3× O(2-).
Die Formel ist dann Al2O3 (Zahlen als Index).
Bei den MolekülIonen (NO3-Nitrat, CO3-Carbonat und PO4-Phosphat) klammert man sie ein, damit der Zahlenindex für das ganze Molekül gilt.

Ich versuche es mal am Beispiel Magnesiumnitrar zu erklären.
Mg 2+. NO3 1-.
Wieviele NO3 Gruppen braucht man nun, damit das ganze elektrisch neutral wird? Richtig, zwei. Denn dann hat man einmal 2+ und zweimal 1- = 2-. Und 2- + 2+ = 0.
In der Strukturformel schreibt man dann Mg(NO3)2, weil die NO3-Gruppe zweimal vorkommt. Man könnte auch MgNO3NO3 schreiben, was aber unübersichtlich ist.