Röntgenspektrum? Kapha Kbeta?
Hallo Leute
Meine Aufgabe bestand darin die Energie für Kalpha und Kbeta mithilfe des Mosley-Gesetzes zu berechnen.
Dabei erhalte ich eine höhere Energie bei dem Kbeta daher das Elektron ja auch von der M Schale auf die K Schale übergeht und bei Kalpha von L auf K.
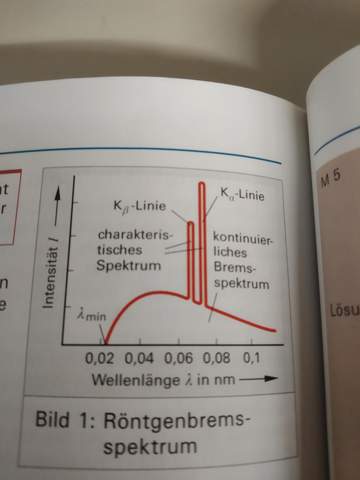
Nun verstehe ich den Zusammenhang jedoch zur folgenden Abbildung nicht daher hier die Intensität von Kbeta kleiner ist als die von Kalpha obwohl doch Kbeta eigentlich Energiereicher sein muss, was verstehe ich falsch?
1 Antwort

Du verwechselst Intensität mit Energie. Intensität bezeichnet im Normalfall die Anzahl der gemessenen Teilchen oder irgendwas was dazu in Abhängigkeit steckt. Deine Energie kommt von der Wellenlänge. Bei Photonen gilt E=h*f bzw E=h*c/lambda wegen f=c/lambda. Daraus folgt, dass Photonen mit großer Wellenlänge weniger Energie haben und kleine Wellenlängen mehr Energie haben. Die Kbeta Linie ist vor der Kalpha Linie und hat somit die geringere Wellenlänge also die höhere Frequenz also die höhere Energie. Also ist deine theoreitsche Erkenntnis durchaus richtig.