Frage zum Gleichgewichtsdiagramm für das Stoffsystem Ethanol / Wasser bei einer Destillation?
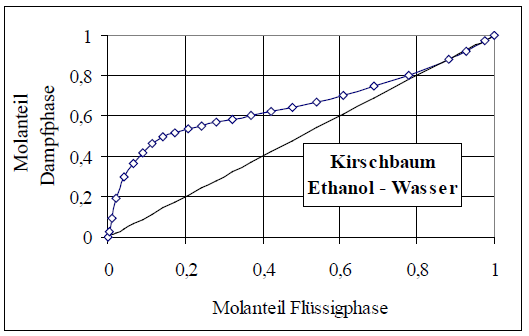
Kann mir einer erklären warum der Trennaufwand bei niedrigen Konzentrationen niedriger ist? Bei steigenden Konzentrationen nähert sich der Wert der Idealen an bis hin zur Azeotropie, d.h. er ist nicht mehr trennbar. Liegt es an den Intermolekularen Kräften und wenn ja welche? Oder liegt es an der Durchmischung? Ich blicke da noch nicht ganz so durch.
2 Antworten

Auf einer Ebene, die in der Schule wohl Teilchenebene genannt wird, liegt der hohe Siedepunkt von Wasser nicht an der Tatsache, dass Wasser stärkere Wasserstoffbrücken ausbildet, sondern dass es mehr ausbildet.
Ein Wassermolekül kann ja 4 Brücken ausbilden, 2 über die H-Atome und 2 über die freien Elektronenpaare. Ethanol hat nur 1 polarisiertes H-Atom, da nützen auch die beiden freien Elektronepaare nichts, er kann nur 2 Brücken bilden.
Was passiert nun mit einem Wassermolekül, das nur von Ethanolmolekülen umgeben ist? Ebent, es kann mangels Partner ebenfalls nur 2 Brücken ausbilden.

Der Unterschied liegt einfach im Dampfdruck, der bei Wasser und tiefen Temperaturen geringer ist als bei Ethanol. Das Destillieren sollte daher bei niedrigen Temperaturen erfolgen.