Wasser-Glycerin-Gemisch?
Hallo!!
Ich habe hier diese Aufgabe:
Erläutere die gute Wasserlöslichkeit von Glycerin in Wasser. Fertige hierzu mittels Strukturformeln eine Skizze von einem Ausschnitt aus einem Wasser-Glycerin-Gemisch an.
Ich weis warum Glycerin sehr gut in Wasser löslich ist und ich kenne auch die Strukturformeln von Glycerin und Wasser, aber ich weis nicht wie dieses Gemisch aussehen muss. Also wie die Wassermoleküle "an" die Moleküle des Glycerin sich heften oder wie das dann aussehen muss.
Ich freue mich über jede Hilfe!!!
Danke!!!!
2 Antworten
Das Stichwort sind (elektrostatische) Coulomb-Wechselwirkungen zwischen Dipolen.
Zeichne dir in deiner Skizze doch einmal die Partialladungen der jeweiligen Moleküle ein. Dann verstehst du auch, was du graphisch anschaulich tun musst.
Erst mal ganz wichtig, es handelt sich nicht um echte Ladungen, wie bei einem Ion, sondern um Partialladungen im Rahmen eines Dipols.
Jetzt bist du doch fast am Ziel. Mach doch bitte dasselbe beim Glycerin, betrachte insbesondere die polaren Hydroxylgruppen.
Und dann erkläre mir, wie eine Dipol-Dipol-Wechselwirkung funktioniert. Dann hast du's.
Bei Glycerin müsste bei der Hydroxygruppe doch auch Sauerstoff negative und Wasserstoff positive Partialladung haben. Heist das jetzt das diese Dipol Dipol Wechselwirkung so entsteht, da die Wasserstoffmoleküle des Wassers vom Sauerstoffmolekül des Glycerin angezogen wird, da dieser eine negative Partialladung hat und die Wasserstoffmoleküle eine positive?
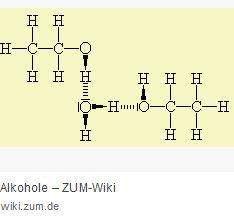
So wie hier ein Ausschnitt aus einem Ethanol-Wasser-Gemisch gezeichnet ist, kannst Du anstelle von Ethanol das Glycerin verwenden und die entsprechenden H-Brücken einzeichnen.

Naja, ich weis das sauerstoffmolekül ist negative geladen und die beiden wasserstoffmoleküle positiv. Ich bin jetzt nicht der beste in Chemie und wüsste nicht was man daraus schlussfolgern kann. Kannst du das bitte genauer erklären.