Warum muss ich Sauerstoff nicht pneumatisch auffangen?
Hallo, ich bräuchte Hilfe bei meiner Chemie Aufgabe, ich komme einfach nicht weiter.
Die Frage ist: warum muss man Sauerstoff nicht pneumatisch auffangen.
Könnte mir da jemand bitte helfen?
2 Antworten
Wenn du ihn nicht pneumatisch auffängst, ist er wegen des geringen Unterschiedes in der Dichte sofort weg und vermischt sich mit der Umgebungsluft.
Anders wäre das bei Kohlendioxid; das ist so schwer, daß es zu Boden sinkt und sogar aus einem Becherglas "umgegossen" werden kann.
Ohne weitere Infos kann man deine Frage also nicht beantworten.
m.f.G.
anwesende
klappt hervorragend auch aus Essig und Karbonat im Reagenzglas. Schräg über ein Becherglas gehalten und dieses danach in eine eine Schale mit zwei unterschiedlich hohen Kerzen. Große Staune-Augen garantiert ;-)
m.f.G.
anwesende
Dass das Umgießen funktioniert hatte ich auch gar nicht angezweifelt - nur die Anreicherung in Nähe des Fußbodens findet nicht statt. Beim Umgießen haben die Luftströmungen zu wenig Zeit, den Vorgang zu stören.
Bringt jetzt nicht viel,wenn ich sage, daß es bei mir regelmäßig klappt und du sagst, daß es das bei dir nicht tut. Einigen wir uns auf unentschieden ;-)
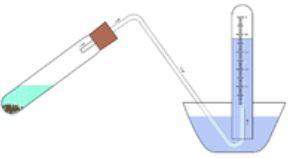
Die folgende bildliche Darstellung würde das pneumatische Auffangen eines Gases zeigen:
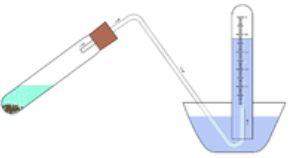
Da der Sauerstoff durch Wasser zum Auffangen geleitet wird, nehme ich an, dass es um die Löslichkeit des Sauerstoffs in Wasser geht.
Die Löslichkeit von Sauerstoff in Wasser ist aber so gering, dass der "Löslichkeitsfehler" in einem Schulversuch zu vernachlässigen ist.
> daß es zu Boden sinkt
Nur in der Theorie - die Luftbewegung in einem Zimmer verhindert das, zumal CO2 meist warm ist, da aus Verbrennung resultierend.. Wenn CO2 trotzdem unten angereichert ist, dann entweder