Chemie Redoxgleichung aufstellen?

Hallo :)
Ich muss im Chemieunterricht eine Redoxgleichung aufstellen und komme leider nicht weiter.
Die Gleichung:
Ch3OH + Cr2O7 -> HCHO+ Cr3+
Wie man auf dem Bild sieht habe ich es versucht, jedoch weiß ich nicht wie der weitere Verlauf aussehen soll.
Vielen Dank im Vorraus!
2 Antworten
Bei der Oxidation eines Alkohols mittels Chromate (hier Methanol) kann es auch passieren, dass komplett bis zum Alkohol durchoxidiert wird. Um das zu vermeiden nimmt man Jones-Reagenz (PCC), das mal zu Beginn, aber zurück zu Deiner Aufgabe.
Für die Oxidation schau Dir mal das C-Atom am Aldehyd an. Du oxidierst Methanol zu Methanal und reduzierst gleichzeitig Cr(VI) zu Cr(III). Das bedeutet, Du hast einen "Nettoaustausch" von zwei mal drei Elektronen (ohne jetzt auszugleichen).
Es ist zwar lange her, dass ich Redoxgleichungen aufgestellt habe, aber irgendwie hab ich das hinbekommen
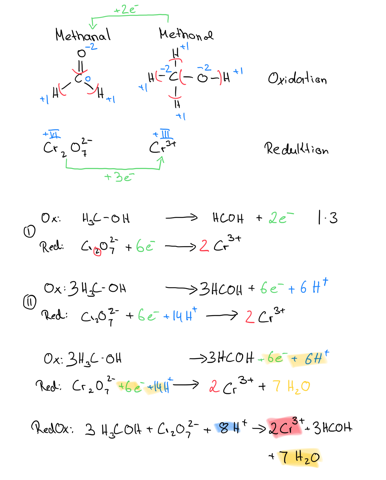
Dass diese Oxidation dadurch nur im Sauren stattfinden kann (oder im sauren pH-Bereich bevorzugt abläuft) brauche ich jetzt nicht extra zu erwähnen ;)
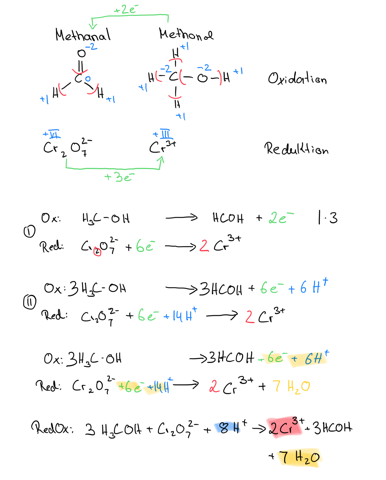
vom dichromat müssen ja der sauerstoffanteil verschwinden und das passiert durch reaktion mit h+ ionen zu wasser. Also für ein O brauchst du jeweils 2h+
desweiteren bestimmst du noch die Oxidationszahlen vom dichromat um herauszufinden wie viele elektronen benötigt werden um 2cr3+ ionen draus zu machen
Außerdem wird bei der ocidation des ethanols wasserstoffionen abgegeben die von wasser unter bildung von h3o+ aufgenommen werden.
Anschließend musst du noch noch die gleichungen so multiplizieren dass du die elektronen wegkürzen kannst und anschließend kürzt du noch h20 und h3o+
in deiner gleichung der oxidation hast du doch selbst geschrieben das dort das da protonen abgeben werden? undobes nunum methanol oder ethanol geht ist doch irellavant weilsich an der der zusätzlichen ch3 gruppe nichts ändert.
und ich habe nur die generelle schritfolge aufgeschrieven wie man da vorgeht und dazu gehören eben auch die oxidagionszahlen...
Nein, Du irrst Dich. Lies bitte nochmal: Es werden Protonen benötigt! Die Reaktion läuft nur im Sauren ab. Das liegt insbesondere daran, dass mit dem Chrom temp. ein Ester oder etwas ähnliches gebildet wird.
du schreibst doch selbst in der redoxgleichung bei der oxidation dass da h+ ionen entstehen???
dass die sich am ende in der gesammtgelichung wegkürzen und insgesammt protonen benötigt werden ist mir klar, aber es ging um die Teilgleichung.
Das habe ich nicht geschrieben. Bitte bring da nichts durcheinander. Schau doch mal genauer hin. Es werden 14 H+ eingebracht. Da kann nichts neues entstehen
Ups, hast ein paar Fehler ;)
Wurde gemacht Cr(VI) zu Cr(III)
Nein, es wird kein Proton abgegeben. Die Reaktion benötigt dringendst Protonen! Zudem geht es um Methanol ;)