Reaktionsmechanismen langsamer und schneller Schritt (Chemie)?
Anscheinend wird hier die Reaktion in Schritte zerlegt, und der erste Schritt ist der Flaschenhals, und der zweite Schritt die bestimmende Geschwindigkeit. Aber irgendwie verstehe ich die beiden Schritte in der Reaktion nicht.
Ich meine, in den 2 Einzelschritten wird NO+F zu ONF gemacht, und insgesamt 2 NO+ F2 zu 2 ONF. Aber wieso ist bei dem mittleren Schritt zu viel und es wird ONF und F gebildet? Ist das nicht ein F zu viel? Ich verstehe gerade gar nichts
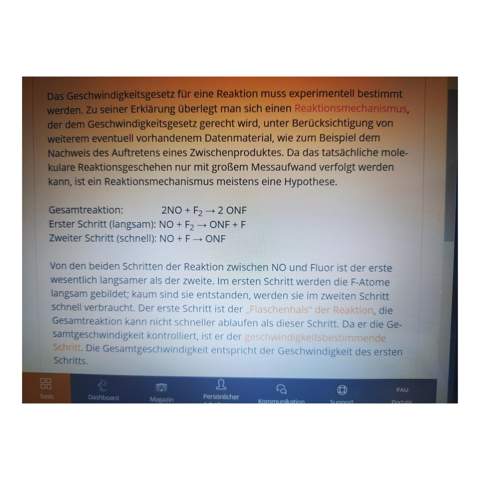
Und wenn es nicht so gemeint ist, dass die 1.+2. die Gesamtreaktion ergeben, sondern zuerst die erste Komma und daraus die zweite abläuft, das macht doch keinen Sinn, wieso soll im ersten schritt ONF+F entstehen und im 2. wieder ONF daraus gemacht werden?
1 Antwort

und der erste Schritt ist der Flaschenhals, und der zweite Schritt die bestimmende Geschwindigkeit.
Falsch. Der 1. Schritt, d. h. der langsamere Schritt ist geschwindigkeitsbestimmend.
Die 2. Reaktion bildet aus NO und F und ONF, ist schneller als die 1. Reaktion und trägt damit relativ (!) gesehen viel effizienter zur ONF Bildung bei, aber deren Geschwindigkeit ist insofern nicht entscheidend, weil ja immer nur so viel F reagieren kann, wie durch die langsame Reaktion gebildet wurde.
Ein bildlicher Vergleich: Du hast 2 Arbeiter. Der langsame Arbeiter öffnet Walnussschalen und produziert aus Walnüssen Walnuskerne und Walnussschalen. Der andere Arbeiter ist super schnell, kann zwar Walnüsse nicht normal öffnen, aber kennt dafür einen Trick wie er mit leeren Walnussschalen ganz einfach geschlossene Walnüsse aufhebelt. Dabei gehen dann aber die Walnussschalen kaputt und er ist darauf angewiesen, dass der langsame Arbeiter erst welche erzeugt. Wenn die Tagesaufgabe beider Arbeiter also lautet so viele Nüsse wie möglich zu öffnen, ist die Geschwindigkeit des schnelleren Arbeiters also irrelevant, insofern seine Geschwindigkeit gedrosselt wird, da er abhängig von der langsamen Arbeit des anderen ist.