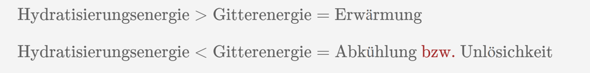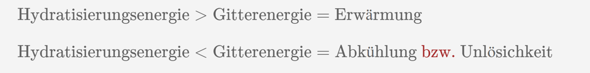Chemie - Löslichkeit Unterschiede von wasserfreien Salzen im Gegensatz zu Salzen mit Kristallwasser?
Chemie - Löslichkeit Unterschiede von wasserfreien Salzen im Gegensatz zu Salzen mit Kristallwasser?
Warum ist die Löslichkeit in Wasser von:
Magnesiunitrat (wasserfrei), Mg(NO3)2 --> 712 g/Lit (25°C)
größer als bei
Magnesiunitrat - Hexahydrat (6 H2O Kristallwasser), Mg(NO3)2 . 6H2O --> 420 g/Lit 712 g/Lit (20°C)
???
BZW. warum ist dies so angegeben?
Müßte es nicht so sein, dass nach Auflösung des wasserfreien und des Kristallwasserhaltigen Salzes die gleiche Menge bezogen auf die gelösten Ionen im Wasser gelöst sind?
Wie ist dies zu erklären?
1 Antwort

Ein Teil des Salzes liegt schon hydratisiert vor somit wird bei der Hydratisierung des Salzes mit Kristallwasser weniger Energie frei, die aber benötigt wird um die Gitterenergie zu überwinden. Somit ist die Löslichkeit von kristallwasserhaltigen Salzen geringer als ihr Anhydrid. Ich weiß nicht ob das immer gilt, aber es gibt sicherlich auch Ausnahmen, aber für dein Salz hier ist das die Erklärung.
Das Lösen von Salzen - Chemie-Schule
Da kannst du den Lösevorgang von Salzen nochmal nachlesen