Kalium -> Kaliumkation/Kaliumion | K+
Lithium -> Lithiumkation/Lithiumion | Li+
Barium -> Bariumkation/Bariumion | Ba2+
Kalium -> Kaliumkation/Kaliumion | K+
Lithium -> Lithiumkation/Lithiumion | Li+
Barium -> Bariumkation/Bariumion | Ba2+
Weil er drei Bindungspartner hat und und deshalb 1 Elektron "zu wenig". Erst wenn er sein Proton, also den Wasserstoff, abgibt ist er neutral.
warum Kokain als chemischer Stoff eine Atombindung darstellt?
Weil sich in diesem Molekül keine Elemente in einer Verbindung befinden, deren Elektronegativitätsdifferenz sehr groß ist, sprich es sind stehts Bindungen zweier Nichtmetalle.
Aus welchen zwei Nichtmetallatomen besteht er?
Man kann es nicht nur als zwei zusammenfassen. Da wären zum Beispiel Kohlenwasserstoffe, eine Bindung aus Kohlenstoff und Wasserstoff. Das sind diese langen Striche, aus dem das Molekülgerüst besteht. Da gibt es dann noch Verbindungen aus Kohlenstoff und Sauerstoff, Kohlenstoff und Stickstoff und natürlich der Kohlenstoff mit sich selbst, gehört aber eher in die Kategorie der Kohlenwasserstoffe.
Das zweite ist richtig. Magnesium ist in der zweiten Hauptgruppe und besitzt die Oxidationsstufe 2 in jeglichen Verbindungen außer mit sich selbst, da ist es 0.
1: Li | Li+ | Cl | Cl- | LiCl
2: Ca | Ca2+ | F | F- | CaF2
3: Al | Al3+ | O | O2- | Al2O3
Keine Ahnung ob das in die 10. Klasse gehört aber Säure und Base ist immer gut :D
Der größte Vorteil von Papierstreifenindikatoren wäre wohl der, dass du damit nicht deine Lösung "verunreinigst" und auch nur ganz kleine Mengen benötigst.

Essigsäure reagiert mit Propanol unter einer Veresterung zum Ethansäurepropylester/Essigsäurepropylester.
Wikipedia hilft dir sicher weiter.
Desto mehr H+ Ionen in der Lösung sind, desto schneller gelingt die Veresterung. Außerdem wird auch so die Ausbeute erhöht, da Ester relativ unlöslich in Wasser sind und nicht so leicht weiter reagieren.
Das ist die Stoffmenge von Eisen.
2g Eisen geteilt durch die molare Masse von Eisen also 55,845 g/mol.
Es gibt durchaus Produkte, die zu einer ausgewogenen Ernährung noch zusätzlich genommen werden können. Das wären so Sachen wie Ashwagandha für besseren Schlaf und weniger Stress oder Kreatin wenn man zusätzlich noch Sport macht aber auch wenn nicht ist es trotzdem vorteilhaft für viele Bereiche in der Gesundheit.
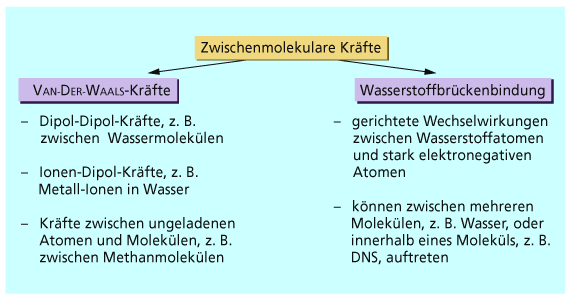
Falls dir das nicht reicht hier etwas genauer:
https://studyflix.de/chemie/zwischenmolekulare-krafte-2392
https://www.helpster.de/wasserstoffbrueckenbindung-und-van-der-waals-kraefte-unterschied_192719#:~:text=Van%20der%20Waals%20Kr%C3%A4fte%20treten,sich%20in%20der%20Elektonenh%C3%BClle%20permanent.
Ja, es gibt andere räumliche Strukturen die einen Dipol bilden können. Beispiel für ein tetraedrisches Molekül wäre NH3.
Gemeinsamkeiten:
Unterschiede:
Das ist die Liste, die ich spontan dazu sagen könnte. Wenn das nicht reicht, kannste ja einfach googlen...
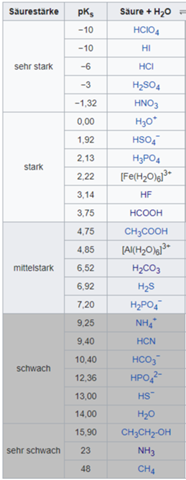
Sehr starke Säuren besitzen einen pKs-Wert von kleiner als −0,35. Starke bis mittelstarke Säuren besitzen einen pKs-Wert von ±0,35
Laut dieser Webseite zwischen 2,5 - 4,5 %
Ist wohl die chlorophyllreichste Pflanze, die man bisher gefunden hat.
An sich könnten die Aussagen aber auch falsch verstanden werden, weil die nicht sachlich genug sind.
Essigsäure + Natriumhydroxid = Natriumacetat + Wasser
2 MnO4- + 6 H+ + 5 NO2- → 2 Mn2+ + 3 H2O+ + 5 NO3-
Das ganze ist halt eine Redoxreaktion. Du musst die 2 Reaktionen, also die Oxidation und die Reduktion aufschreiben, um deine Koeffizienten zu ermitteln. Dazu musst du zuerst die Oxidationszahlen herausfinden.
Hier ein Video wie du das machst:
https://www.youtube.com/watch?v=lAnDb_lTfoE
Oder du machst das ganze einfach mit probieren... geht manchmal sogar schneller.
PS: Nettes Interface... sieht nach allgemeiner Chemie der RUB aus :D
Die Menge von ca. 90g Eiweiß die du beschreibst bezieht sich ja auf die Gesamtmenge an Eiweiß die du brauchst. Der Proteinshake hilft dir nur dabei, diesen Wert zu erreichen sofern du die Menge nicht mit der Nahrung decken kannst. Demnach reicht ein Proteinshake am Tag schon aus, da der Rest schon mit der Ernährung kommen sollte... heist also, dass deine 600g Packung für gut 20 Tage reichen sollte sofern du nur eine Portion am Tag nimmst.