Wie berechne ich die Elektronegativitätsdifferenzen von Ethanol?
Ich habe diese aufgabe in Chemie aufbekommen und ich weiß nicht mehr weiter... kann mir jemand dabei helfen?

1 Antwort

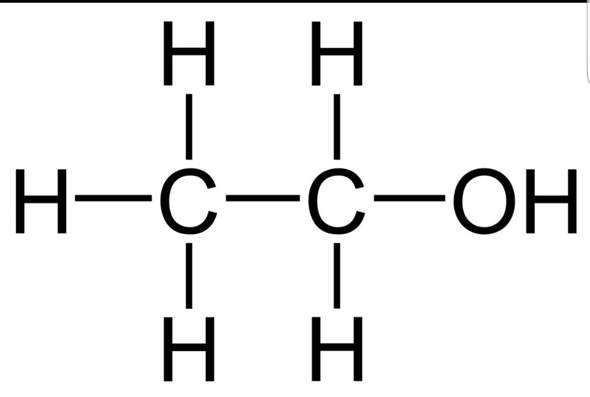
In Ethanol gibt es ja vier verschiedene Bindungen. Einmal die Bindung von Kohlenstoff zu Wasserstoff, dann noch die Bindung von Kohlenstoff zu Kohlenstoff, die Bindung von Kohlenstoff zu Sauerstoff und noch die Bindung von Sauerstoff zu Wasserstoff. Um dir das klarzumachen, hilft es, wenn du dir mal die Strukturformel des Moleküls aufzeichnest. Hier mal ein Bild der Strukturformel von Ethanol:
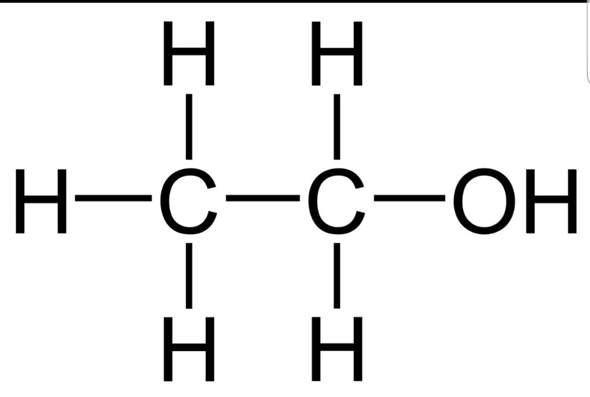
Entscheidend für die Polarität von Atombindungen, ist die Elektronegativitätsdifferenz. Jedes Atom hat eine Elektronegativität. Die Elektronegativität gibt an, wie stark die Fähigkeit eines Atoms ist, die Bindungselektronen anzuziehen. Die Elektronegativitätadifferenz bestimmst du, indem du den Unterschied der Elektronegativitäten berechnest, die an der Bindung beteiligt sind. Liegt die Elektronegativitätadifferenz zwischen 0 und 0,4, handelt es sich um eine unpolare Atombindung. Ist sie zwischen 0,4 und 1,7, ist es eine polare Atombindung. Und ist die Elektronegativitätsdifferenz größer als 1,7, liegt eine Ionenbindung vor. Diese Werte sind allerdings nicht als starre Grenzwerte zu verstehen, denn der Übergang ist fließend.
Ich mache das jetzt mal exemplarisch für die Bindung zwischen dem Sauerstoff- und dem Wasserssersroffatom. Sauerstoff hat eine Elektronegativität von 3,4 und Wassersroff eine Elektronegativität von 2,2 (kannst du in deinem Periodensystem oder im Internet nachschauen). Die Elektronegativitätsdifferent ist also 1,2. Damit handelt es sich um eine polare Atombindung.