Zeichnung einer Titrationskurve einer basischen Aminosäure?
Hi, ich habe folgende Frage.
Wie sieht die Zeichnung einer Titrationskurve einer basischen Aminosäure aus.
Und in welcher Molekülform die basische Aminosäure in den einzelnen pH-Bereichen vorliegt.
Danke im Voraus :)
1 Antwort

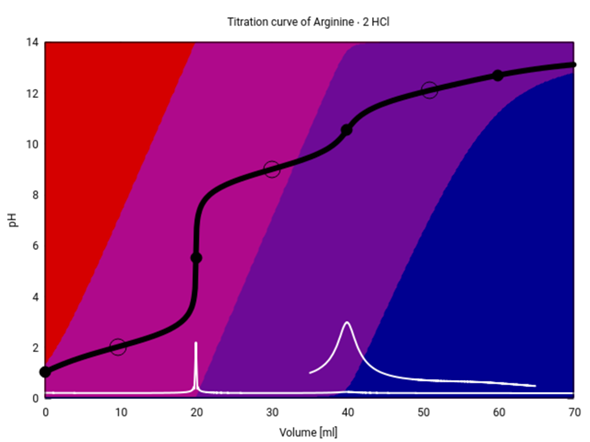
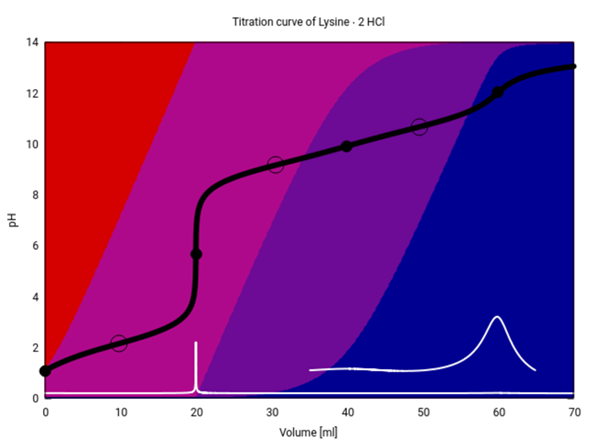
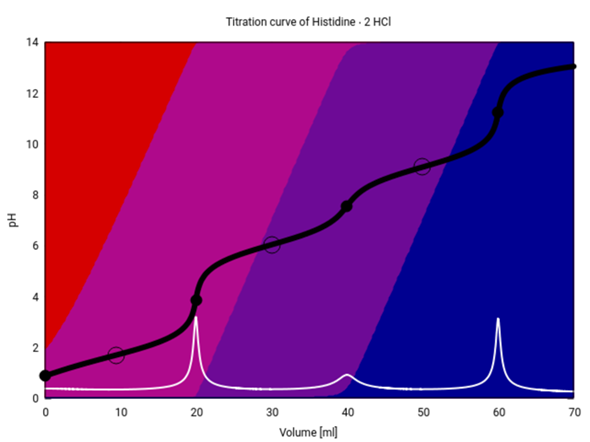
Hier hast Du die Titrationskurven für Arginin, Histidin und Lysin. Titriert werden jeweils 20 ml einer 0.1 mol/l Lösung der vollkommen sauren Spezies (also des Dikations) mit 0.1 mol NaOH. Die verwendeten pKₐ-Werte sind:
Arginin: 2.03, 9.00, 12.10
Histidin: 1.70, 9.9, 6.04
Lysin: 2.15, 9.16, 10.67
Die schwarze Kurve ist die Titrationskurve; Äquivalenzpunkte sind mit Kreisen, Pufferpunkte (pH=pKₐ) mit Ringen eingezeichnet. Die weiße Kurve ist die erste Ableitung der schwarzen, ggf. mit Vergrößerungen. Die Hintergrundfarben codieren die Speziesverteilung: rot =Dikation, rotviolett=Monokation, blauviolett=Zwitterion, blau=Anion.
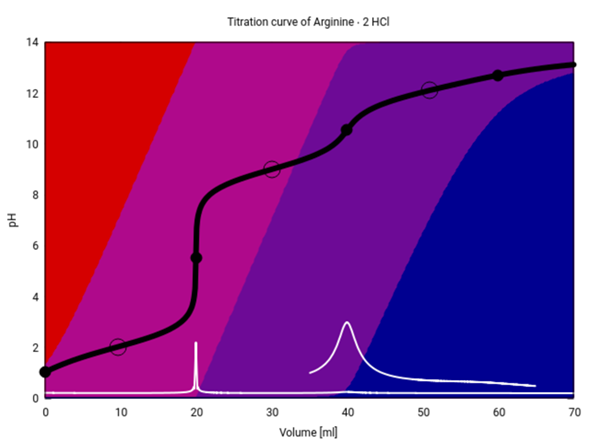
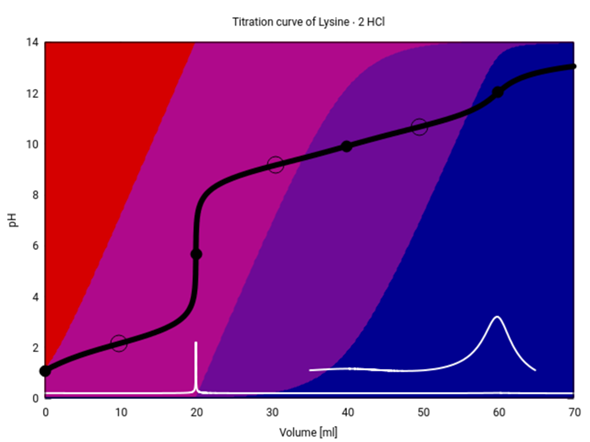
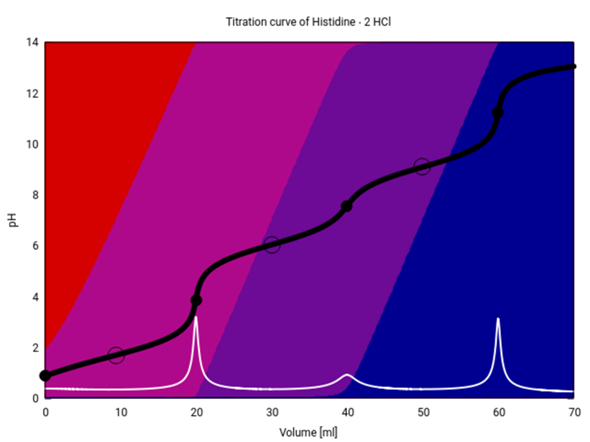
Du siehst, daß Histidin aus der Reihe tanzt — das liegt natürlich daran, daß die zweite Deprotonisierung nicht wie bei den anderen beiden von der α-Aminogruppe (bzw. Ammonium in der Säureform) kommt, sondern von der Seitenkette. Bei Histidin ist ja das Seitenketten-N (im Heterocyclus) weniger basisch als das α-N, und umgekehrt ist das protonierte N in der Seitenkette die stärkere Säure (vgl. pKₐ-Werte oben).
(Ich habe das jetzt schnell und unter Zeitdruck heruntergerechnet, aber eigentlich sollte es stimmen. Wenn Dir was fischig vorkommt, bitte nachfragen).