Woran erkenne ich, ob ein Molekül ein Dipol ist?
Woran erkenne ich bei der Lewis-Schreibweise von NO2, ob NO2 ein Dipol ist?
Die Lewis-Schreibweise von NO2 ist ja folgende:
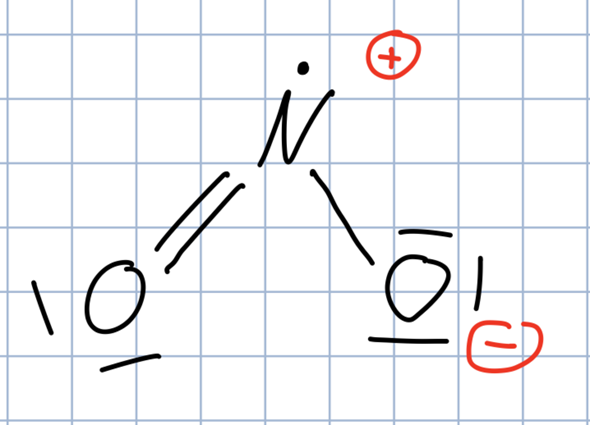
Vielen Dank
1 Antwort

Hi,
Für einen Dipol brauchst du eine polare Bindung oder eine echte Ladungstrennung.
Dazu dürfen die Schwerpunkte der Ladung nicht zusammenfallen.
Jetzt erkennst du es sicher selbst, ob es ein Dipol ist oder nicht.
m.f.G.
anwesende

Mit den Ladungsschwerpunkten hast du recht, aber du hast die erste Bedingung vergessen. Schau mal nach der EN von O und N.
(Danach auch noch H. Dann schaust du hier und vergleichst H2O und NO2:)
https://www.spektrum.de/lexikon/chemie/dipolmoment/2563
m.f.G.
anwesende

Ah, dann dürfte NO2 kein Dipol sein, da ∆EN von O und N ≈ 0,4 ist, weshalb NO2 unpolar ist und es somit überhaupt keine zwei Pole gibt, damit sich ein Dipol bilden kann.
Wäre NO2 aber polar, wäre es ein Dipol, da die Ladungsschwerpunkte wegen der gewinkelten Raumstruktur nicht zusammenfallen, oder?
Danke für die Antwort :)
Also müsste es sich um einen Dipol handeln, da die Ladungsschwerpunkte in einer gewinkelten Raumstruktur, wie der von NO2, nicht zusammenfallen, oder?