Was ist ein Dipol-Molekül?
4 Antworten

Moin,
das ist ein Molekül, das einerseits Bindungspartner enthält, die durch eine polare Atombindung miteinander verbunden sind UND in dem gleichzeitig die beiden Teilladungsschwerpunkte durch die Molekülgeometrie auf zwei Seiten verteilt sind.
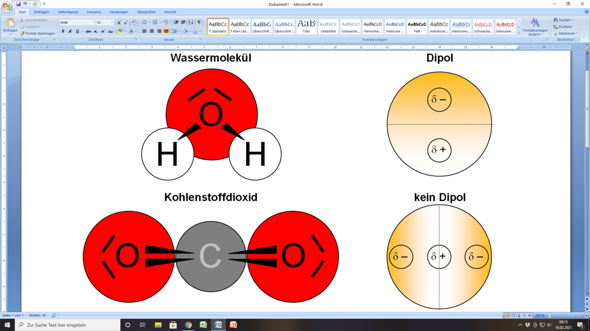
Beispiel Wasser (H2O):
Zwischen Wasserstoff (H) und Sauerstoff (O) liegt eine polare Atombindung. Die Molekülgeometrie ist gewinkelt. Wenn du dir das Molekül als Kugel vorstellst, gibt es deshalb eine Halbkugel, die eine negative Teilladung hat, und eine Halbkugel, die eine positive Telladung hat. Eine Kugel mit zwei entgegengesetzt teilgeladenen Polen, ein Dipol.
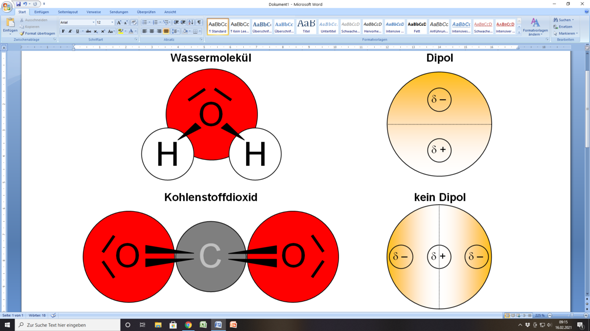
Beim Kohlenstoffdioxid gibt es zwischen Sauerstoff (O) und Kohlenstoff (C) ebenfalls polare Bindungen. Aber das Molekül ist linear gebaut, wobei die beiden Sauerstoffatome außen und das Kohlenstoffatom im Zentrum liegen. Wenn du dir dieses Molekül als Kugel vorstellst, entstehen zwei Pole, die die gleiche negative Teilladung haben (und am Äquator liegt das positiv teilgeladene Zentrum). Es sind also keine entgegengesetzte Teilladungen an den Polen, sondern die gleichen Teilladungen. Daher ist Kohlenstoffdioxid kein Dipol.
Ein Dipolmolekül muss erst einmal polare Atombindungen haben. Aber das allein reicht noch nicht aus. Die dadurch entstehenden Teilladungen müssen auf unterschiedliche Seiten des Moleküls verteilt sein. Erst beides zusammen ergibt ein Dipolmolekül.
Alles klar?
LG von der Waterkant

Ein Dipol-Molekül ist ein ist eines, dass durch partielle Ladungsverschiebung zwei schwächere Pole ausbildet. Es gibt im Internet genug soclher Erklörungen und Videos...

Was ist ein Dipol-Molekül?
