Redoxreaktion aufstellen und Potential berechnen?
Ich stehe gerade auf dem Schlauch, was das Aufstellen der Redoxgleichungen folgender Aufgabe aufgeht, und frage mich auch, wie ich das Potentail von BrO3- -->HOBr berechnen soll, wenn ich im Prinzip dafür ja nur ein gesichertes Potential (also das von BrO3- --> Br-, 1,4 V) habe, nach der Lutherschen Regel aber zwei benötige?
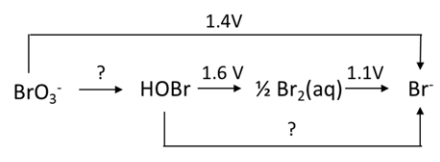
"Formuliere die Reduktionsgleichungen für die Reaktionen von BrO3 - -->HOBr und HOBr -->Br- in saurer Lösung und berechne die E0 -Werte für diese Reaktionen."
Danke im voraus
2 Antworten

Manchmal kann es helfen, stattdessen mit den Gibbs-Enthalpien zu rechnen:
dG = - z F E
Von Bromat zu Hypobromit 4 e-, Hypobromit zu Brom und Brom zu Bromid je 1, insgesamt +V -> -I.


Formuliere die Reduktionsgleichungen für die Reaktionen von BrO3 - -->HOBr ...
1) BrO3⁻ + 4 e⁻ + 5 H3O⁺ → HOBr + 7 H2O
2) 2 HOBr + 2 e⁻ + 2 H3O⁺→ Br2 + 4 H2O
3) Br2 + 2 e⁻ → 2 Br⁻
Das Redoxpotential für 1) beträgt 1,45 V.

Danke. Aber wie kann ich mit der Gibbs-Enthalpie rechnen, wenn diese nicht gegeben ist?