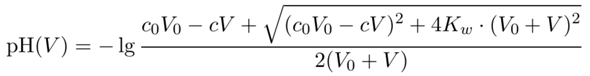Ph POH etc?
Wie soll man die folgende Aufgabe lösen? Ich hab bei der Ausgangslösung verstanden, dass man den negativen dekadischen Logarithmus ziehen muss, wie geht es jedoch
PS: Es handelt sich hier nicht um eine Hausaufgabe, sondern ich war an dem Tag nicht in der Schule und bereite mich nun auf die Klausur vor


1 Antwort

Zum Auswerten der Titration: Du verbraucht V=10 ml einer c=1 mol/l NaOH, das sind n=cV=10 mmol. In den V=100 ml HCl muß also gleich viel Stoffmenge HCl enthalten gewesen sein, daher ist die Konzentration der Salzsäure c=n/V=0.1 mol/l.
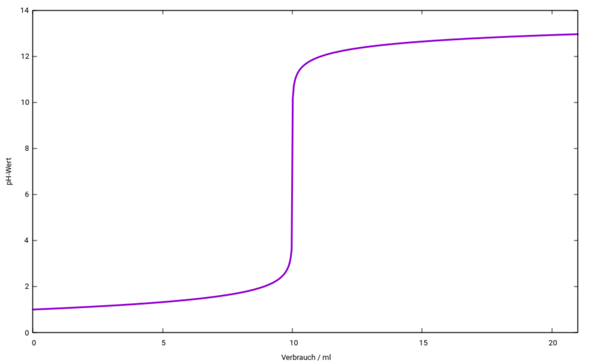
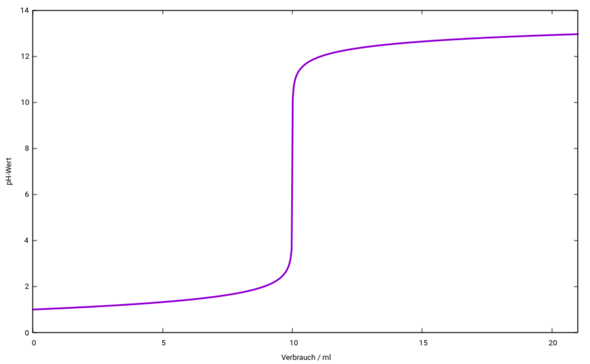
Das ist Deine Titrationskurve. Die von Dir berechneten pH-Werte liegen nicht genau auf dieser Kurve, und ich weiß nicht, warum das so ist. Richtig sind für
V= 0, 1, 9, 10, 11, 19, 20
pH = 1, 1.05, 2.04, 7, 11.95, 12.87, 12.92
Da Du nicht sagst, wie Du das ausgerechnet hast, kann ich nur raten, was Du getrieben hast (wenn ich raten muß: Hast Du vielleicht nicht berücksichtigt, daß das Volumen im Kolben immer mehr wird?). Vielleicht willst Du mir ja einen Punkt (z.B. V=19 ml) genau vorrechnen. Ich bekomme meine Zahlen mit
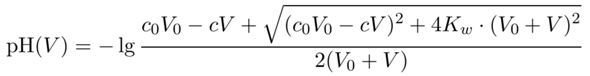
wobei c₀=0.1 mol/l und V₀=100 ml sich auf die HCl beziehen, V und c=1 mol/l auf die NaOH.
Deine Angaben für c(H₃O⁺) usw. sind richtig, aber warum schreibst Du z.B. 10¯¹·⁰⁵ und nicht 0.089? Das ist doch viel besser lesbar.