pH- Wert von pkb berechnen?
53g Diethanolamin werden in 2 L Wasser geöst. Was ist der pH Wert? pkb= 5.12
- Es werden noch 20ml 10M HCL hinzugefügt was ist der pH-Wert
- Es werden nochmal 20ml 10M HCL hinzugefügt was ist der pH-Wert
2 Antworten

Für schwache Basen gilt:
pH = ½ (pKs + log cB + 14) und
pKs + pKB = 14
cB = 0,252 mol/L
pH = 11,14
Den Rest habe ich gelöscht, weil ich Konzentration und Stoffmenge durcheinander gemixt hatte. Richtige Antwort s. indiachinacook!

Diethanolamin C₄H₁₁NO₂ hat die molare Masse M=105.14 g/mol. Folglich entsprechen Deine m=53 g einer Stoffmenge n=m/M=0.504 mol, und die Stoffmengenkonzentration in den 2 l Lösung beträgt folglich c=n/V=0.25 mol/l. Daraus berechnet man einen pH=11.14. Dazu kannst Du die dieselben Formeln benutzen, die ich Dir in meiner letzten Antwort gegeben habe; Du mußt dabei die Säurekonstante durch die Basenkonstante ersetzen und die Formel liefert dann nicht den pH, sondern den pOH, den Du erst in den pH umrechnen mußt (pH=14−pOH).
Wenn Du 20 ml zehnmolarer HCl zufügst, dann kommen 0.2 mol HCl dazu. Von den ursprünglichen 0.504 mol Diethanolamin werden also 0.2 mol zum Diethanolammonium-Kation reagieren, und 0.304 bleiben übrig. Den pH-Wert kann man näherungsweise mit der Henderson-Hasselbalch-Gleichung berechnen, die in diesem Fall lautet
pH = 14 − pKb + lg (Base/Salz), wobei Du für die Base das Diethanolamin und für das Salz das Diethanolammonium einsetzen mußt; dabei mußt Du nicht die echten Konzentrationen ausrechnen, es reichen die Stoffmengen. Das Resultat ist pH=9.06.
Mit 40 ml funktioniert es ganz gleich, und Du bekommst als Resultat pH=8.30
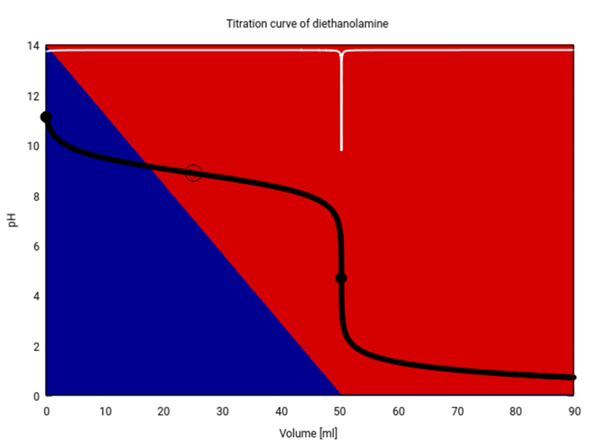
Natürlich könnte man sich auch fragen, wie das für beliebige Mengen HCl aussieht, und ich zeige Dir, wie das Resultat aussieht. Die von Dir berechneten pH-Werte findest Du bei V=0, 20 und 40 ml. Die schwarze Kurve ist der pH in Abhängigkeit von der zugegebenen Säuremenge. Du siehst, daß der pH springt, wenn gleich viel Stoffmenge von Diethanolamin und HCl in der Suppe herumschwimmen (bei ca. 50.4 ml), weil dann alles Diethanolamin (blauer Hintergrund) verschwindet, und die Suppe nur noch Diethanolammonium-Ionen (roter Hintergrund) enthält.
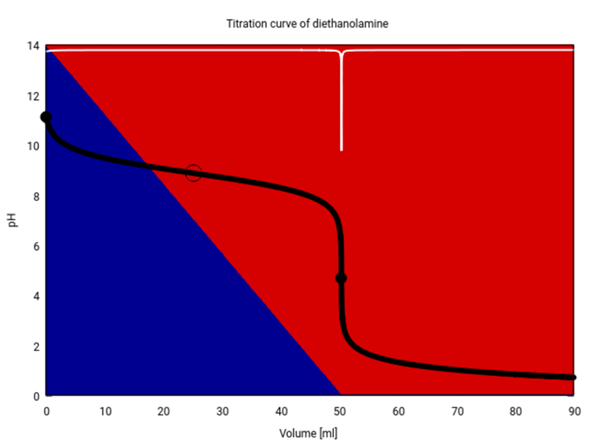

bzw. wieso rechne ich nicht mit der normalen pOH Formel: pOH=pkb - log (c)/2 und dann ph= 14-pOH (wieso haben Sie, das durch 2 ausgelassen)?

Vermutlich meinst Du die zweite Berechnung (bei Zusatz von 20 ml HCl).
14 − 5.12 +lg (0.304/ 0.2)
8.88 + lg (1.52)
8.88 + 0.18
9.06

ich weiß nicht, was Du mit „normale Formel“ meinst. https://de.wikipedia.org/wiki/Henderson-Hasselbalch-Gleichung

hallo, wie komme ich auf die ph=9,07 ich habe es öfters durchgerechnet und mir kommt immer nur ph= 9,7