pH Wert berechnen?
Sie mischen zu 20ml einer 0,01 molaren zweiwertigen Säure, bspw. H2SO4, 20ml 0,005 molares NaOH. Wie ist der Ph-Wert? pKs = 4,22
1 Antwort

Ich verstehe nicht, was Deine Angabe „pKₛ = 4.22“ bedeuten soll — sie paßt jedenfalls nicht zur Schwefelsäure (pK₁≈−3, pK₂=1.99). Letztlich muß eine zweibasige Säure ja zwei pKₐ-Werte haben. Also ignoriere ich das und rechne mit Schwefelsäure.
Wir haben n=cV=0.2 mmol zweibasiger Säure H₂SO₄ plus 0.1 mmol NaOH, die reagieren zu 0.1 mol NaHSO₄, und 0.1 mol H₂SO₄ bleiben übrig. Beides schwimmt in 40 ml Flüssigkeit, also bekommen wir eine Lösung mit c(NaHSO₄)=c(H₂SO₄)=n/V=0.0025 mol/l.
Der pH ist nicht ganz trivial auszurechnen, denn man braucht das Massenwirkungsgesetz dazu. Da H₂SO₄ eine starke Säure ist, werden die 0.0025 mol/l H₂SO₄ mit dem Wasser zu ebensoviel H₃O⁺ plus HSO₄⁻ reagieren; aber HSO₄⁻ ist ja auch eine Säure und wird teilweise mit dem Wasser zu H₃O⁺+HSO₄⁻ reagieren. Wieviel H₃O⁺ insgesamt gebildet werden, ist nicht ganz leicht zu sehen.
Was man sofort sagen kann:
- Aus der H₂SO₄ bekommen wir 0.0025 mol/l H₃O⁺, die kann uns keiner mehr wegnehmen.
- Wir haben dann insgesamt 0.005 mol/l HSO₄⁻ in der Suppe, die liefern weitere H₃O⁺, aber maximal 0.005 mol/l (weil ja nicht mehr da ist)
- Also muß gelten 0.0025 ≤ c(H₃O⁺) ≤ 0.0075 mol/l, bzw. 2.60 ≥ pH ≥ 2.12
Wenn man es richtig ausrechnet, dann kommt pH=2.24 heraus. Die Formel, mit der das geht, habe ich kürzlich hergeleitet, aber für einen etwas allgemeineren Fall. Sie lautet
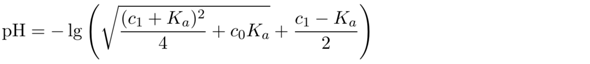
Wobei c₀=0.005 mol/l die Gesamtkonzentration von Schwefelsäure und HSO₄⁻ ist und c₁=0.0025 mol/l die reine Schwefelsäurekonzentration. Kₐ ist in diesem Fall die zweite Säurekonstante der Schwefelsäure, also Kₐ=10⁻¹·⁹⁹≈0.01 mol/l. Einsetzen liefert den pH=2.24.
Wenn Deine rätselhafte Angabe „pKₛ = 4.22“ sich auf die Säurekonstante der zweiten Protolysestufe der zweibasigen Säure beziehen soll, dann lautet das Ergebnis übrigens pH=2.58; das liegt daran, daß in diesem Fall die zweite Säurestufe so schwach ist, daß sie fast keine H₃O⁺-Ionen mehr beiträgt. Deshalb hätte man sie auch gleich vernachlässigen können und sich mit dem oben angegebenen Schätzwert 2.60 zufriedengeben können.