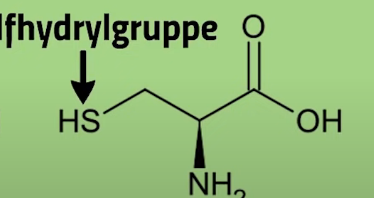
Warum sorgt die Sulfhydrylgruppe bei Aminosäuren für eine Polare Restgruppe, wenn doch die EN- Differenz von S und H nur 0,2 ist?
1 Antwort

Hallo NimaM750,
rein qualitativ kann ich mir vorstellen, dass das O-Atom in der COOH-Gruppe eine große Elektronegativität vorweist - und damit trotz einer anwesenden Thiol-Gruppe mit eigener kleineren Elektronegativität dominant ist.
In wässriger Lösung wird auch eher das H-Atom der OH-Gruppe dissoziieren - wobei sich über die Thiol-Gruppen immerhin Schwefelbrücken bilden lassen.
Mit vielen lieben Grüßen
EarthCtizen