Wann bindendes Elektronenpaar, wann freies?
Hey :)
Sitze gerade an Chemie und da hab ich mich gefragt, wann eigentlich ein Elektronenpaar als bindend oder frei betrachtet wird
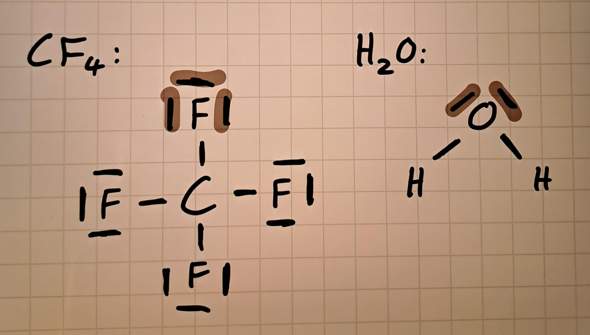
Ein freies EP kann sich noch verbinden, ein bindendes nicht, das ist mir klar. Aber inwievern unterscheiden sich die markierten Elektronenpaare auf dem Bild voneinander? Bei H²O sind die anscheinend frei, wieso dann nicht bei CF⁴? Was unterscheidet die denn, oder bin ich einfach nur unnötig verwirrt?
Danke jedenfalls im Voraus :D
2 Antworten

Ja, Du bist unnötig verwirrt. Freie Elektronen(paare) sind definitionsgemäß diejenigen Valenzelektronen, die nicht an einer Bindung beteiligt sind. Es ist auch nicht richtig, dass freie Elektronenpaare zwangsläufig für weitere Bindungen zur Verfügung stehen. In dem speziellen Beispiel kann das Fluor keine weiteren Bindungen eingehen. Der Sauerstoff am Wassermolekül nimmt allerdings gerne noch ein Proton auf, wobei ein Elektronenpaar verwendet wird. Ein zweites Proton kann theoretisch auch zum H4O²⁺ führen, ist aber in der kondensierten Phase praktisch nicht möglich. In der Gasphase sind meiner Kenntnis nach solche Exoten allerdings stabil. Das ist für die Chemie an der Schule jedoch ohne Relevanz.

Die markierten Elektronenpaare beim F sind genauso freie Elektronenpaare wie die markierten beim O.

Ja schon, warum sollten die sich unterscheiden? Sind in beiden Fällen ungebundene Elektronenpaare
Uff, echt? Danke dann :)