Säure-Base-Titration?
Hallo zusammen, ;)
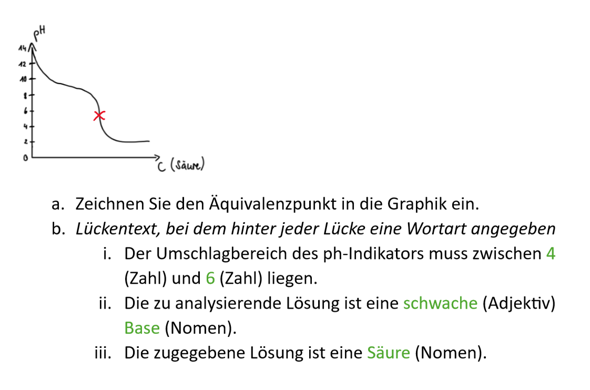
ich hab eine Frage zu folgender Aufgabe:
Woran erkenne was die analysierende und was die zugegebene Lösung ist?
1 Antwort

Hi,
das kannst du daran erkennen, wie der Graph der Titration sich entwickelt.
Würdest du eine Säure mit einer Base titrieren, so würde der pH-Wert kontinuierlich ansteigen. Zunächst ist in der Probenlösung nur die Säure drin, der pH-Wert ist also gering. Je mehr Base dazu kommt, desto mehr H(+)-Ionen reagieren zu Wasser ab – bis zum Äquivalenzpunkt: Ab da sind dann die OH(-)-Ionen durch die Base im Überschluss vorhanden, sodass der pH-Wert weiter ansteigt.
Wird die Base vorgelegt und dann mit der Säure titriert, so ist der pH-Wert durch den starken Überschuss an OH(-)-Ionen hoch. Je mehr Säure hinzugegeben wird, desto mehr fällt der pH-Wert, bis zum Äquivalenzpunkt – danach fällt er weiter, da dann die OH(-)-Ionen der Base abreagiert sind und die H(+)-Ionen im Überschuss vorhanden sind.
Hier fällt der Graph, also liegt in der Probenlösung eine Base vor. Diese wird mit einer Säure titriert.
LG

Vielen Dank!