PH wert von NH4Cl berechnen?
Hallo, ich will denkt- Wert berechnen .. muss ich einfach -log(0,2) rechnen oder ist es komplizierter ?
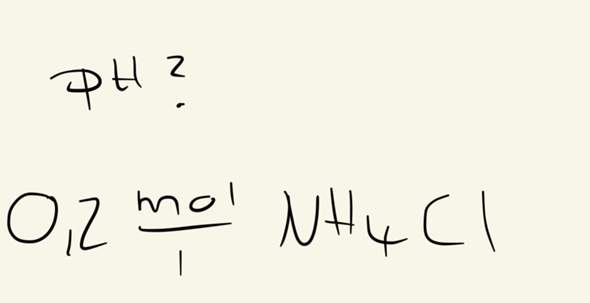
Danke für die Hilfe !

Ich habe es mal anders probiert, wäre es so richtig ?
3 Antworten

Tipp: Das Ammonium-Kation wird ein Proton abgeben. Daher also den pKs-Wert von diesem zur Hilfe nehmen.

Der pKs-Wert vom Ammoniumkation ist 9,25. Ich habe 4,97 raus ;)

komplizierter!
Es ist ja keine starke Säure, sondern ein saures Salz!
Man braucht den pKs des Kations und eine andere Formel!

Hier kannst nicht einfach die Definition des pH Werts der starken Säure nehmen sondern die Henderson Hasselbalch Gleichung
pH = 1/2 (pKs - lg c0)
Weil die Lösung als schwache Säure reagiert
Hcl=starke Säure
Ammoniak ist eine Schwache Base

Richtiger Weg, aber als HH Gleichung bezeichnet man die Puffergleichung!

Dachte das beide Gleichungen so heißen weil sie voneinander abgeleitet sind
Hat den diese Gleichung auch einen Namen?

Also ich kenne keinen! Für mich ist das einfach die Gleichung für saure Salzlösungen.
Abstammen tun die alle vom MWG und der Autoprotolyse von Wasser.
Nicht jede Gleichung wird da gleich nach ihrem Entdeckter beannnt.

Ich habs mal mit der Gleichnung probiert, kannst du mal gucken ob ich’s richtig gemacht habe ? ( siehe oben )

Wenn du den pks Wert richtig ausgerechnet hast ist dein pH Wert auch richtig


Das stimmt natürlich auch wollte aber sagen das die Gleichung richtig verwendet worden ist

Aber das richtige Ergebnis ist sowieso 4.97448500217 für den pH Aber der Fragesteller kommt wegen dem falschen pKs Wert nicht darauf
Danke, ich habe es mal anders probiert, kannst du mal kontrollieren ( siehe oben )