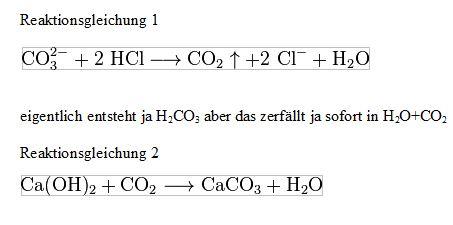
Löslichkeitsprodukt bei carbonat nachweis
Wie ich schon in meiner letztesn frage erklärt habe muss ich einige nachweise ausarbeiten und bin momentan an dem carbonat nachweis.( https://www.gutefrage.net/frage/carbonat-nachweis---gleichgewicht? ) ich habe zu beiden reaktionsgleichungen ein Löslichkeitsprodukt aufgestellt, ich weiß jedoch nicht ob es stimmt und ob ich hinter den bruch ein >1 oder <1 schreiben muss... es ware nett wenn ihr sie kontrollieren könntet :)
danke jued
P.S. bei der ersten Reaktion bin ich mir nicht sicher ob ich als produkt H2CO3 oder H2O+CO2 nehmen soll, deswegen habe ich hier zwei varianten... und muss ich bei der ersten reaktion überhaupt ein löslichkeitsprodukt aufstellen?


2 Antworten

bei der ersten Reaktion bin ich mir nicht sicher ob ich als produkt H2CO3 oder H2O+CO2 nehmen soll, deswegen habe ich hier zwei varianten... und muss ich bei der ersten reaktion überhaupt ein löslichkeitsprodukt aufstellen?
Das Löslichkeitspordukt betrachtete nur den Lösungsvorgang, nicht für die weitere Reaktion (der Zerfall von Kohlensäure). Ins MWG gehen Feststoffe übrigens nicht mit ein.
ich habe zu beiden reaktionsgleichungen ein Löslichkeitsprodukt aufgestellt, ich weiß jedoch nicht ob es stimmt und ob ich hinter den bruch ein >1 oder <1 schreiben muss.
Einfache selbst überlegen:
Ein >1 bedeutet, der Term im Zähler ist größer als der im Nenner, <1 genau das Gegenteil.
Was ist bei dir der Fall?

KL = [A+]^n · [B-]^m
Du musst oben die Produkte und unten die Edukte schreiben.
Das Problem ist, dass sich das MWG für die Löslichkeit nicht so schön aufstellen lässt, denn die Kohlensäure zerfällt in wässriger Lösung sofort bzw liegt ebenfalls gelöst vor, nämlich als Ionen. Nimmst du tatsächlich das Löslichkeitsprodukt von H2CO3 müsstest du durch 0 teilen und das darf man nicht (ohne komplexe Zahlen ..). Man müsste also anders an diese Löslichkeit heran gehen, ich denke aber nicht, dass das hier nötig ist. Man könnte die Kohlensäure auch stationär als Feststoff annehmen, mein erster Gedanke, aber das ist keine gute Näherung meines erachtens.
Ich würde daher das Löslichkeitsprodukt weglassen und einfach das allgemeine MWG für beide Reaktion aufstellen, da musst du einfach alle Produkte oben und alle Edukte unten hin schreiben und die stöchometrischen Zahlen als Koeffizienten.

ok also damit ich das jetzt auch richtig verstanden habe: bei der ersten reaktion mache ich ein MWG, aber welche pordukte nehme ich denn dann? also kohlensäure oder CO2 und wasser?
und bei der zweiten reaktion kann ich das KL so nehmen wie ich es aufgestellt habe oder soll ich da auch ein MWG aufstellen? und das gleichgewicht müsste bei der reaktion doch auf seite der produkte sein weil das CaCO3 ja ein feststoff ist und nur schwerlöslich ist und somit die rückreaktion nur schlecht abläuft oder?

Bei Reaktionen in wässriger Lösung lässt man die Konzentration des Wassers meist weg. Und bei Fällungsreaktionen die Konzentration des Feststoffs, die ist per Definition 1.
Damit ergibt sich als Löslichkeitsprodukt des Calciumcarbonats:
KL = [Ca++] * [CO3--]
mit "mal" und nicht mit plus, deshalb heißt es ja auch Löslichkeitsprodukt
Die Gleichung zur Kohlensäure vergessen wir besser wieder. Hat erstens nichts mit Löslichkeitsprodukt zu tun, sondern mit Dissoziation. Zweitens kann man eine zweistufige Reaktion (H2CO3 -> HCO3- -> CO3--) nicht so einfach in eine einzige Gleichung packen.
Für die Kohlensäure wäre die Dissoziationskonstante ein guter Ausgangspunkt.

ja stimmt mal statt plus :D
kann es sein das ich die ganze zeit KC und KL verwechselt habe?

kann es sein das ich die ganze zeit KC und KL verwechselt habe?
Möglich, aber das erklärt nicht wirklich die Fehler, denn auch bei KC (soll doch wohl die Konstante aus dem MWG sein?) stehen in Zähler und Nenner Produkte, keine Summen. (Summen bildest Du manchmal bei Berechnungen, z.B. wenn Du etwas Essigsäure in Wasser gibst: Summe der Acetat-Ionen plus der undissoziierten Essigsäure im Gleichgewicht ist gleich der zugegebenen Menge Essigsäure.
Das Löslichkeitsprodukt ist nur ein Spezialfall des Massenwirkungsgesetzes, bei dem die Konzentration (bzw. Aktivität, falls Ihr den Begriff schon hattet) des Feststoffs auf 1 gesetzt wird.

ja jetzt ist mir das auch auf gefallen das mit dem + ist mir schon total oft passiert danke für den hinweis! und ich habe jetzt auch verstanden wo mein fehler lag wegen kc/kl und so weiter und habe es (hoffentlich richtig) geändert... :) ich musste meine ausarbeitung heute abgeben mal sehen ob ich die versuche jetzt richtig erklärt habe oder nicht :)
also ich würde sagen das ist des KL der ersten reaktion ist dann das wo c(H2CO3) oben steht und ich denke da müsste <1 stehen weil ich ja mehr edukte wie produkte habe weil die kohlensäure ja sofort zerfällt und bei der anderen reaktion müsste es dann >1 sein oder? und was soll mir das sagen, das keine feststoffe eingehen, den tipp verstehe ich nicht... :D heißt das ich muss von der ersten reaktion gar kein KL aufstellen weil das carbonat ein feststoff ist?