Gilt die Oktetregel?
Folgendes Problem: Die Oktetregel sagt aus das alle (eher die meisten) Atome eine Edelgaskonfiguration erreichen wollen mit 8 Elektronen in der äussersten schale. Aber Schwefel und Phosphor zum Beispiel haben 10 elektronen in der äussersten schale wenn sie eine Verbindung eingehen. Wenn jetzt die frage kommt stimmt die Oktetregel für eine Verbindung welche Phosphor mit 10 Elektronen hat, ist die Antwort dann ja oder nein? Wird die Oktetregel verletzt?

Da gilt die Oktettaufweitung zum Beispiel bei
PCl3

dann wäre also die antwort: nein die Oktetregel gilt nicht sondern deren aufweitung
1 Antwort

Moin,
die Oktettregel ist ein unglückliches Überbleibsel und sollte meiner Meinung nach nicht mehr benutzt werden.
Für Wasserstoff gilt diese Regel ohnehin nie! Und auch die Ionen von Lithium (Li^+) oder Beryllium (Be^2+) haben in ihrer äußeren Schale ebenfalls keine acht Elektronen, weil in die K-Schale nun einmal nur zwei Elektronen hinein passen.
Die Oktettregel gilt relativ streng ohnehin nur für die Elemente der 2. Periode im PSE ab Kohlenstoff. Das sind gerade einmal C, N, O und F! Und selbst da gibt es im Falle von Stickoxiden Ausnahmen (siehe Stickstoffmonoxid oder Stickstoffdioxid).
Bei etlichen anderen Elementen in Verbindungen gilt sie zwar oft, aber manchmal eben auch nicht (zumindest nicht in üblichen Lewis-Formel-Darstellungen).
Wenn du zum Beispiel das Schwefelsäure-Molekül nimmst, dann findest du oft diese Darstellung:
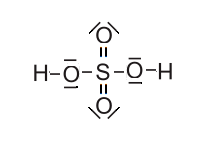
Aber hier hätte das Schwefelatom sogar 12 Valenzelektronen... Das könnte man mit folgender Darstellung lösen:
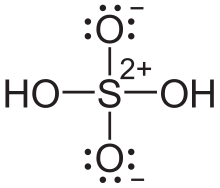
Hier gehorchen alle Atome der Oktettregel (bis auf Wasserstoff, natürlich). Doch in dieser Darstellung muss man eben mit Formalladungen arbeiten.
Das geht natürlich, weshalb man am Konzept der Oktettregel festhalten kann. Andererseits... na ja, du kennst meine Meinung ja mittlerweile.
LG von der Waterkant
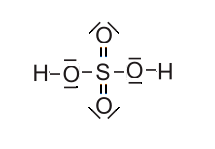
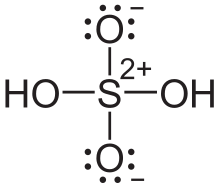


Die Oktettregel gilt relativ streng ohnehin nur für die Elemente der 2. Periode im PSE ab
Das wichtigste :)