Es ist ein Cycloalkan
Du brauchst grundsätzlich die Potentialdifferenz E0, welche du aus der Redoxreaktion ableiten kannst.
Mit der Nernstgleichung kannst du die Konzentrationsabhängigkeit der Energie berechnen. E0 ist die Potentialdifferenz, laut Wikipedia sind das 2.04V.
R ist die Gaskonstante, ca. 8.31J/(mol*K).
T ist die Temperatur in KELVIN. Diese sollte gegeben sein.
z ist die Zahl der übertragenen Elektronen, das sollten hier 2 Elektronen sein.
F ist die Faradaykonstante, welche ca. 96485 C/mol groß ist.
c(Ox) und c(Red) sind die Konzentrationen des oxidierten bzw. reduzierten Reaktionspartners, also Pb(4) und Pb(2). Diese müssen ebenfalls gegeben sind.
Das ist noch nicht das Ende der Geschichte: Wird der Akku aufgeladen oder entladen?
Ist die Temperatur 25°C? Dann kann die Gleichung noch vereinfacht werden.
Ist die Lösung nicht stark verdünnt? Dann müssen wir nämlich die Gleichung ebenfalls verändern.
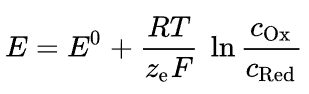
Den Rest können wir erst mit ein paar Informationen beantworten.
Lg
Enantiomere verhalten sich wie Bild und Spiegelbild.
Diastereomere verhalten sich nicht wie Bild und Spiegelbild.
Epimere sind Diastereomere, aber nicht alle Diastereomere sind Epimere.
Epimere besitzen mindestens zwei Stereozentren, aber unterscheiden sich an nur einem Stereozentrum. Hat ein Molekül nur ein Stereozentrum ist es kein Epimer.
Ein Beispiel wäre das Verhältnis von D-Glucose zu D-Mannose: Sie besitzen vier Stereozentren (in dem Fall OH-Gruppen), welche in der Fischer-Projektion entweder rechts oder links liegen.
Bei D-Glucose liegt nur (von oben gezählt) die zweite OH-Gruppe links, bei Mannose sind es die erste und die zweite OH-Gruppe. Alle anderen OH-Gruppen liegen rechts. Egal wie du Glucose spiegelt, es ist nicht das Spiegelbild der Mannose. Das ist der Unterschied zu den Enantiomeren: D-Glucose ist das Spiegelbild der L-Glucose.
Anomere sind ein Spezialfall der Epimere. Bei Anomeren liegt der Unterschied an dem Kohlenstoff, welcher eine Carbonylgruppe (Keto- oder Aldehydgruppe) trägt.
Von Anomeren spricht man meistens nur in der Kohlenhydrat- bzw. Zuckerchemie, und diese Moleküle haben mehrere chirale Zentren.
Aber ja, an sich ist es schon richtig, dass man nicht will, dass Diastereomere auch Enantiomere sind. Die beiden Begriffe beschreiben eine unterschiedliche Art der Isomerie.
Ich hoffe, deine Fragen haben sich jetzt geklärt :)
Chloroform - das wirkt aber in der Realität weder so schnell noch so effektiv.
Hallo,
Ich denke, du bringst hier zwei Sachen durcheinander: Den Dipol und das Dipolmoment.
Der Dipol selbst hängt nur von den verknüpften Atomen und deren Elektronegativität ab.
Ich gebe dir jetzt eine vereinfachte Beschreibung:
Hast du beispielsweise einen Kohlenstoff, welcher mit einem weiteren Kohlenstoff verknüpft ist, sind die Elektronen beziehungsweise die Ladung gleich verteilt, es gibt keinen Dipol.
Ist der Kohlenstoff aber mit einem Element verknüpft, welches eine andere Elektronegativität hat, sind die Elektronen nicht gleich verteilt. Ein Beispiel: Kohlenstoff in Bindung mit dem stark elektronegativen Fluor: Hier werden die Elektronen vom Fluor angezogen und sich hauptsächlich dort aufhalten: Du hast einen Dipol.
Jetzt zum Dipolmoment:
Dieser ist von der Molekülgeometrie abhängig. Bei CO2 werden die Elektronen in Richtung des Sauerstoffs gezogen. Da das Molekül aber völlig gerade wie ein Stock (=linear) ist und sich links und rechts vom Kohlenstoff ein Sauerstoff befindet liegt zwar ein Dipol vor, das Dipolmoment ist aber null. Wasser (H2O) andererseits hat die beiden Wasserstoffatome auf einer Seite und deswegen einen Dipolmoment.
Ein Beispiel ist 1,2-Dichlorethen.
Bei der Cis-Verbindung schauen die beiden elektronegativen Chloratome in eine Richtung und ziehen auch die Elektronen in eine Richtung. Es liegt ein Dipol und ein Dipolmoment vor, die Ladung ist gerichtet.
Bei der Trans-Verbindung stehen sich die Chloratome gegenüber: Sie ziehen gleichmäßig in unterschiedliche Richtungen. Es gibt also wieder einen Dipol, aber kein Dipolmoment.
Falls du noch Fragen hast kannst du sie mir gerne stellen.
Shepan versucht viele Server zu betreten, vermutlich ist da ein Scam dahinter - er versucht auch mehrmals täglich meinen zu betreten.
Ich würde dir empfehlen die Whitelist auf deinem Server zu aktivieren, dann kann er nicht mehr beitreten.