Habe eine Frage zu der Lewis-Schreibweise in Chemie (9. Klasse Realschule).
Das Element brom hat 35 Elektronen und steht in der 7. Periode, also müsste es 7 Elektronen auf der außenschale besitzen. Wenn ich jedoch rechne 35-2-8-8-8-8=1 (zwei Elektronen auf der innersten schale und auf jeder weiteren 8), müsste das bedeuten, dass auf der außenschale nur 1 Atom ist. Was ist jetzt richtig?? Und wie schreibt man es in der Lewis Schreibweise? Ich hoffe, ihr könnt mir helfen und bedanke mich schon im voraus :)
4 Antworten

Und Übrigens: Brom steht in der 7. Hauptgruppe und in der 4. Periode. :-T
Die allgemeine(n) Rechnung(en) müsste(n) lauten:
(1 ≤ Ordnungszahl ≤ 2) = Anzahl Valenzelektronen (= "A.Ve"; für nachher)
(3 ≤ Ordnungszahl ≤ 10) = [Ordnungszahl] - 2 = A. Ve
(11 ≤ Ordnungszahl ≤ 18) = [Ordnungszahl] - 2 - 8 = A. Ve
(19 ≤ Ordnungszahl ≤ 36) =
[Ordnungszahl] - 2 - 8 - 10 + [Wenn "Ordnungszahl" = (19 oder 20); = 2] = A. Ve
(37 ≤ Ordnungszahl ≤ 54) =
[Ordnungszahl] - 2 - 8 - 18 - 10 + [Wenn "Ordnungszahl" = (37 oder 38); = 2] = A. Ve
(55 ≤ Ordnungszahl ≤ 86) =
[Ordnungszahl] - 2 - 8 - 18 - 18 - 24 + [Wenn "Ordnungszahl" = (55 oder 56); = 2] = A. Ve
(87 ≤ Ordnungszahl ≤ 118*) =
[Ordnungszahl] - 2 - 8 - 18 - 18 - 32 - 24 + [Wenn "Ordnungszahl" = (87 oder 88); = 2] = A. Ve
*Die Elemente nach Plutonium (Ordnungszahl 94) sind alle künstlich hergestellt, die Elemente 113 (Ununtrium), 115 (Ununpentium), 117 (Ununseptium) und alle Elemente mit Ordnungszahlen ≥ 119 noch gar nicht entdeckt worden.
Ich hoffe, ich konnte helfen :-)
LG Tobi! :-D


Das Element brom hat 35 Elektronen
Im atomaren Grundzustand.
und steht in der 7. Periode,
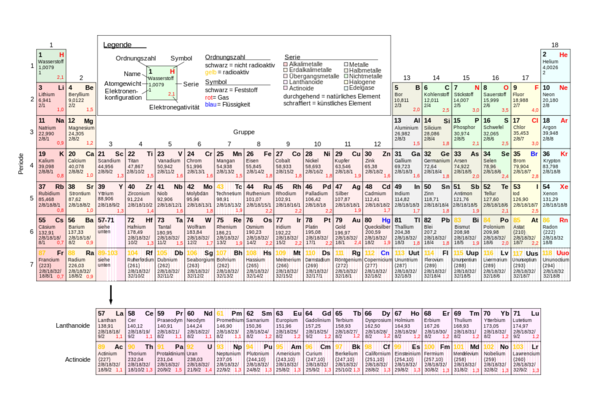
Falls du dich auf das PSE beziehst: Falsch. 4. Periode, 17. Gruppe.
also müsste es 7 Elektronen auf der außenschale besitzen. Wenn ich jedoch rechne 35-2-8-8-8-8=1 (zwei Elektronen auf der innersten schale und auf jeder weiteren 8), müsste das bedeuten, dass auf der außenschale nur 1 Atom ist.
Du rechnest falsch. Ehe die p-Elektronen der 4. Periode aufgefüllt werden kommen die d-Elektronen der 3. dran.

Du hast die 10 in der 4. Periode befindlichen Übergangsmetalle nicht mitgezählt.
––> 35 - 2 - 8 - 8 - 10 ((Erd-)alkalimetalle nicht mitzählen!) = 7
Ich hoffe, ich konnte helfen. :-)
LG Tobi :-D

Vielen Dank für die Antwort, davon habe ich noch nie etwas gehört, da unser Lehrer es nicht gesagt hat. wenn ich also die Lewis Schreibweise anwenden muss, schaue ich am besten nur nach der Lage im Periodensystem, oder?

Für die Lewis-Schreibweise ist nur die Zahl der Außenelektronen relevant. Und das sind 7, wegen der siebenten Hauptgruppe (Halogene).
Wieviele Elektronen da noch „weiter innen drinnen“ sind, spielt in der Chemie meist keine Rolle.
Muss dich enttäuschen. Von113, 115 und 117 sind bereits mehrere Isotope bekannt.