Elektronenaufteilung im Schalenmodell (Chemie)?
Hi, ich hätte eine Frage zu der Elektronenaufteilung beim Schalenmodell bei Nebengruppen. Bitte erst alles von mir lesen, um meine eigentliche Frage dann zu verstehen.
Also in den Hauptgr. ist es bei Calcium ja z.B. so, dass die Elektronen theoretisch in 2, 8, 10 aufgeteilt werden könnten. Da es aber in der 4. Periode ist, benötigt man 4 Schalen. Man nimmt also 2 Elektronen (weil es ja 2. Hg ist) und macht es in die naechste dann hat man 4 Schalen
So und bei den Nebengruppen nehmen wir mal Eisen als Beispiel. Da sind sie so aufgeteilt:
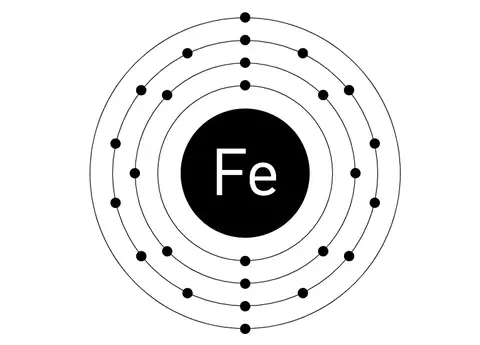
Da es ja auch in der 4. Periode ist brauchen wir 4 Schalen. Hier nimmt man sich dann 2 Elektronen und packt die dann in die nächste Schale. Aber warum 2? Woher weiß man das? Bei den Hauptgruppen guckt man ja einfach in welcher Gruppe es ist, aber wie findet man es bei den Nebengruppen heraus?
Mit freundlichen Grüßen Weißbrot
1 Antwort

Ich fass mich kurz: Das Schalenmodell ist absolut unzureichend für die Nebengruppen. Man kann damit nichts mehr anfangen.
Ganz grob: Es gibt noch "Unterschalen" (Orbitale), die da besetzt werden. Es sind dadurch immer 2 Elektronen, die in der äußersten (bei Fe in der 4.) Schale sitzen. Der Rest ist dann in der Schale darunter. Also Beispiel Ni: 1. Schale 2, 2. Schale 8. Dann 4. Schale wieder 2. Die restlichen 16 sind dann in der 3. Genauso bei Eisen: 2, 8, 14, 2.