Chemie Lewis Struktur richtige Anordnung?
Ich habe das Molekül CF2H2 und soll jetzt eine Lewis Struktur zeichnen.
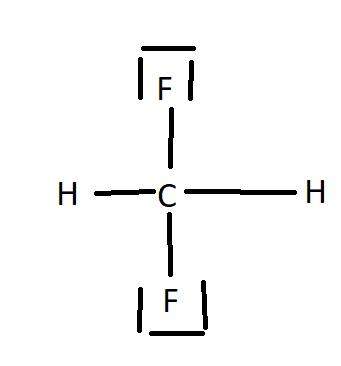
Gibt es eine Regel, welche mir sagt, wie die Anordnung von F und H sein muss.
- Warum ist das zweite F(oder H) gegenüber dem anderem F?
- Warum geht nicht F und gegenüber H?
1 Antwort

Diese Unterschiede in der Anordnung sind bedeutungslos; daher kanst Du das Molekül zeichnen, wie du willst. In Wahrheit ist CH₂F₂ dreidimensional gebaut, und die H- und F-Atome kommen an den Ecken eines näherungsweise regulären Tetraeders zu liegen. Für den Eckpunkt eines Tetraeders gibt es aber kein „gegenüber“ oder „daneben“, sondern die anderen drei liegen alle gleich weit vom ersten entfernt.

Du hast recht, aber nur, wenn das Molekül wirklich flach wie eine Flunder wäre. Solche Moleküle gibt es tatsächlich, berühmt ist das Pd(NH₃)₂Cl₂, da gibt es beide Varianten: Die Chloratome nebeneinander (⇒Dipolmoment) oder gegenüber (⇒unpolar).
Beim CH₂F₂ ist das aber nicht so. Das Molekül ist dreidimensional (hier siehst Du es gezeichnet), und es gibt nur eine mögliche Anordnung der Substituenten. Diese Struktur ist mit einem Dipolmoment verträglich. Als Erfahrungswert gilt, daß Fluoralkane generell hohes Dipolmoment haben (wenn die Struktur eines erlaubt), sich aber trotzdem eher unpolar verhalten.
Je nach Anordnung wär es polar oder unpolar ne? (wegen symetrie)