Chemie schnellere Methode um Molekül Geometrie zu ermitteln?
Momentan mache ich es so:
Wenn ich zum Beispiel IF4- in das AXE Schema bringe muss und die Struktur benenne soll rechne ich erstmal die Valenzelektronen zusammen: 36.
Dann zeichne ich einmal die Lewis Struktur und ordne die 18 Paare entsprechend an, da Iod weit unter der zweiten Periode liegt kann es hypervalent sein, die Anordnung mit den wenigsten Formalladungen ist also die hier:
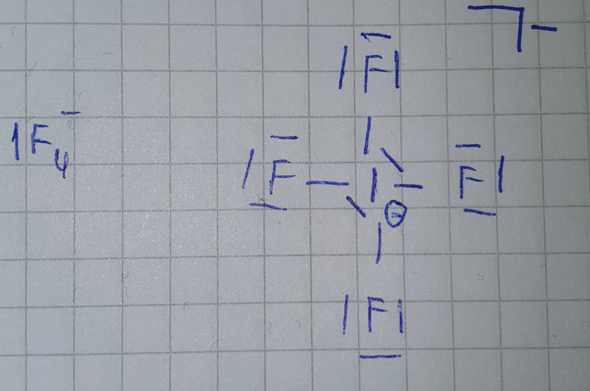
Jetzt weiß ich, dass das Zentralatom 2 einsame Elektronenpaare hat, daraus ergibt sich AX4E2 --> quadratisch-planar.
Gibt es eine Formel, mit der man zum Beispiel direkt die einsamen Elektronenpaare berechnen kann? Das dauert so sonst immer ewig
2 Antworten

Ich weiß nicht, ob es sinnvolll ist, alle Valenzlektronen zu zählen. Nimm an, du würdest 2 F-Atome durch 1 O-Atom ersetzen (kp, ob es IOF₂⁻ gibt), dann hättest du nur 28 Valenzelektonen und würdest trotzdem auf 2 freie Elektronenpaare am Iod kommen. Weniger würden die freien Elektronepaare in der Peripherie, am F bzw. O, 8 statt 12.
Wenn du das aber weißt, wie viele freie Elektronenpaare bei den Anhängen sind, kann du das auch gleich berücksichtigen:
Iod hat 7 VE, eines kommt aus der negativen Ladung, ein F-Atom steuert eines zur Bindung bei, ein O-Atom 2.
So kommst du in jedem Fall auf 12 Elektronen und bei 4 Bindungen auf 2 freie Elektronenpaare.
Beim IF₄⁻ kommst du so auf eine oktaedrische, beim IOF₂⁻ auf eine trigonal-bipyramidale Anordnung. Dass sich die freien Elektronenpaare gegenüberstehen, ist wohl die Regel.

Das Iod hat sieben Außenelektronen, ein achtes kommt durch die negative Ladung dazu. Vier davon bilden Bindungen mit den Fluoratomen, die vier verbleibenen Elektronen schließen sich zu zwei nichtbindenden Elektronenpaaren zusammen. Also landen wir beim Scheme AF₄E₂, folglich ist das Molekül quadratisch–planar.