wie Bestimmt man welchen Indikator man für die Säure braucht?
Muss man die Tabelle auswendig lernen ?
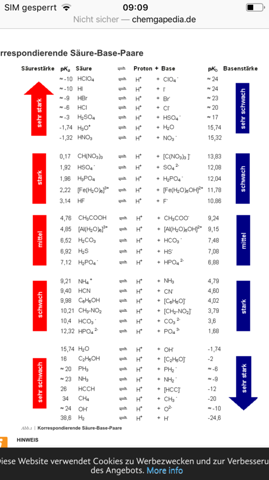
Welchen Indikator nehme ich zbm:
H2 + H- —> ?
H2 + PO4^3- —> H2 + H2PO4^3-
OH- + HS- –> H2O + S-
CH4 + F- —> CH3 + HF
NH3 + NO3- —> NH2 + HNO3
ich weiß nicht wie ich es ausgleiche und ich es richtig aufgestellt habe
also was nehme ich wenn ich sehr schwache Säure + starke base
sehr schwache Säure + Mittel base
sehr schwache Säure + schwache base
sehr schwache Säure + sehr schwache base ist eigentlich der bromthymolblau ?
Schwache Säure + sehr starke Base
Schwache säure + starke Base
.....
wie erkenn ich welchen Indikator ich nehmen soll ?
1 Antwort

Zunächst einmal zum Auswendiglernen der Tabelle: Es wäre schade, wenn euch euer Lehrer*in so eine Tabelle auswendig lernen lasen würde, denn das kann nicht der Sinn eines Chemieunterrichts sein. Es genügt meiner Meinung nach, wenn Du Beispiele für je eine starke und schwache Säure und Base hast.
Der andere Teil Deiner Ausführungen sind unklar bzw. alle Reaktionsgleichungen falsch.
Es geht wahrscheinlich für Dich darum zu wissen welchen Indikator man verwendet um den Äquivalenzpunkt bei der Titration einer Säure (stark oder schwach) mit einer Base (stark oder schwach) zu erkennen.
Poste hier also noch einmal ein Problem, das Dich zu dieser Thematik interessiert.

So wie ich die Aussage Deiner Lehrerin verstehe, will sie wissen, welche Farbe ein bestimmter Indikator anzeigt, wenn er in die Lösung einer bestimmten Säure oder Base gegeben wird.
Das Problem ist aber, dass die Konzentration der Lösung angegeben werden muss.
Beispiel: Eine Essigsäurelösung der Konzentration c = 1 mol/L hat einen pH = 2,4. Der Indikator Methylorange wäre rot gefärbt. Verdünnt man die Lösung, dann ändert sich die Indikatorfarbe nach Gelborange.
Angenommen, es liegen Lösungen der Konzentration c = 1 mol/L vor, dann zeigt Methylorange bei schwachen und sehr schwachen Säuren die Farbe Gelborange und bei mittel bis starken Säuren die Farbe Rot.
Bei den Basen ist der Indikator bei Lösungen (c = 1 mol/L) von schwachen und sehr schwachen Basen farblos und bei stärkeren Basen rotviolett.

welche Farbe ein bestimmter Indikator anzeigt, wenn er in die Lösung einer bestimmten Säure oder Base gegeben wird.
Ich glaube eher "Du hast Säure a und titrierst mit Lauge b. Welchen Indikator verwendest Du, um den Äquivalenzpunkt zu ermitteln?"
Da sollten es reichen, wenn man drei Indikatoren kennt für die pH-Werte 4, 7 und 10.

Dieser Deiner Meinung bin ich auch (s. meine Antwort ganz oben).
Also in der Arbeit meinte meine Lehrerin das wir Säuren und Basen bekommen werden und Ihre Indikatoren bestimmen müssen