Was sind Ionenverbindungen und Salze Hilfe?
Hey Leute ich hätte eime Frage zur Chemie z.b wenn metalle und nicht metalle reagieren entstehen Ionen bindungen. Und Ionen sind geladenen teilchen die wie die Edelgase sein möchten oder? Deshalb nehmen die Elektronen auf oder Ab also Kation und Anion
Und was sind jetzt Salze und Ionenverbindungen? Also emsteht ein Salz wenn z.b die Verhältnisformel neutral ist? Also z.b NaCl beides ist ja 1 erkennt man dadurvh das ein Salz entstanden ist?
3 Antworten

Ionenbindung
Der Ionen-Begriff ist vom griechischen Wort ión (das Wandernde) abgeleitet. Positiv geladene Ionen werden als Kationen bezeichnet, sie entstehen, wenn Atome Elektronen abgeben. Negativ geladene Ionen bezeichnet man als Anionen, sie entstehen, wenn Atome Elektronen aufnehmen. Die Ladungsunterschiede bewirken eine elektrostatische Anziehungskraft zwischen den beiden Ionen. Es entsteht eine Ionenbindung. Die Ionenladung zeigt an, wie viele positive oder negative Ladungen ein Ion besitzt. Sie wird durch eine rechts neben dem Ion hochgestellte, arabische Zahl angegeben. Ist die Ladung nur einfach, wird nur ein Plus- oder ein Minuszeichen geschrieben. Zusammengesetzte Ionen können mit einer eckigen Klammer umfasst werden.
Na+
Natrium-Ion
Mg2+ Cl−
Magnesium-Ion
Cl−
Chlorid-Ion
[SO4] 2−
Sulfat-Ion
Die Ionen bilden ein regelmäßiges Ionengitter. Bei der Natriumchloridstruktur ist im Ionengitter jedes Na+-Ion von sechs Cl−-Ionen oktaedrisch umgeben (in der Grafik verdeutlicht). Gleichzeitig ist auch jedes Cl−-Ion von sechs Na+-Ionen oktaedrisch umgeben. Salze, die nach der Natriumchloridstruktur kristallisieren, können nicht nur Würfel, sondern auch Oktaeder ausbilden.
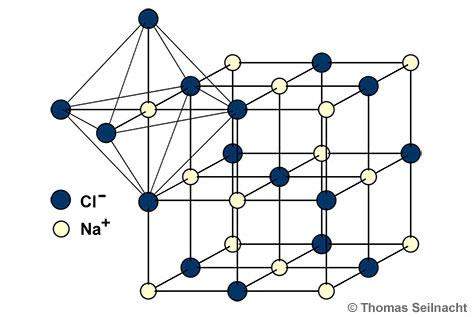
Wird Natriumchlorid im Wasser gelöst, bleiben die Ionen erhalten, sie schwimmen dann frei als Ladungsträger in der Lösung. Aus diesem Grunde leitet salzhaltiges Wasser den elektrischen Strom, während reines, destilliertes Wasser fast keinen Strom leitet. Der Zerfall des Ionengitters in frei bewegliche Na+- und Cl−-Ionen beim Lösungsvorgang ist eine Dissoziation. Etwas vereinfacht formuliert versteht man unter einer Dissoziation den Zerfall einer chemischen Verbindung in zwei oder mehrere Komponenten.
Salze
Im alltäglichen Sprachgebrauch meint man mit dem Begriff Salz das Kochsalz, das im Haushalt eine große Rolle spielt. In der Chemie werden Stoffe als Salze bezeichnet, die aus positiv geladenen Kationen und negativ geladenen Anionen aufgebaut sind und im festen Zustand eine Ionenbindung eingehen und ein Ionengitter bilden. Nach dieser Definition sind die meisten anorganischen Feststoffe Salze. Zu den Salzen zählen zum Beispiel die Carbonate, die Chloride, die Nitrate, die Phosphate oder die Sulfate. Sie kommen in der Natur in großer Zahl in den Mineralien vor und bilden oft schön ausgeformte Kristalle.
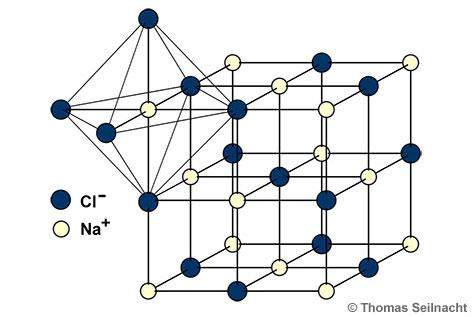

"Ionenverbindung" und "Salz" sind nur verschiedene Worte für die selbe Sache.
Übigens heißt es Ionenverbindung. Eine Verbindung ist ein Stoff, der aus mehr als einem Element besteht. Eine Bindung ist das, was die Teilchen zusammen hält. Nicht unbedingt logisch, aber so ist die Sprache halt.
Viele Ionen erreichen die Elektronenanordnung von Edelgasen, aber längst nicht alle. Außerdem sind nicht alle Verbindungen aus Metall und Nichtmetall Ionenverbindungen und nicht alle Ionenverbindungen bestehen aus Metall und Nichtmetall. Die Gegenbeispiele musst du jetzt noch nicht kennen, aber du solltest im Hinterkopf behalten, dass es immer etwas komplizierter wird.
NaCl ist ein einfaches Beispiel. Das Natiumatom gibt ein Elektron ab und wird so zum Kation Na⁺, das die Elektronenanordnung von Neon hat. Jedes Chloratom nimmt ein Elektron auf und wird so zum Chlorid-Anion Cl⁻ mit der Elekronenanordnung von Argon. Zusammen, im Verhältnis 1:1, bilden sie dann das neutrale Salz.
Das ist ein einfaches Beispiel, und genau das solltest du dir merken.

Nein, das Verhältnis hängt von den Ladungen ab. Magnesium bildet z.B. Kationen mit zweifach positiver Ladung, Mg²⁺. Daher brauchst du pro Magnesiumion 2 Chloridionen, damit das Salz neutral ist. Die Formel für Magnesiumchlorid ist daher MgCl₂.

Ein Salz ist der Stoff. Oder die Stoffkategorie. Die Ionen Bindung beschreibt die Art der Bindung. Das macht Sinn wenn du dir noch andere Bindungsarten anschaust... In der Organischen Chemie Teilen sich die Atome oft beide die Elektronen die die Bindung ermöglichen, bei der Ionenbindung werden die Elektronen tatsächlich abgegeben.
Erstmal vielen dank kann ich mir des auch so merken immer wenn ein Verhältnis 1:1 das es ein neutraler Salz ist?