Warum kann Co2 Infrarotstrahlung so gut absorbieren und was hat das mit dem Dipolmoment zu tun?
2 Antworten

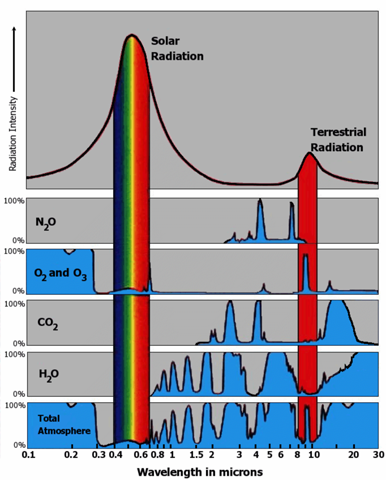
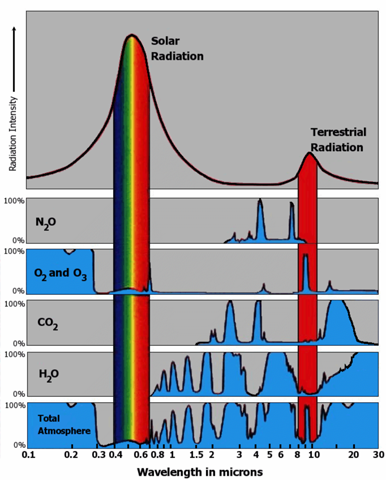
So sonderlich gut absorbiert CO2 Infrarot auch nicht, ist ja ein Gas und hat damit nur einzelne Bereiche, in denen es gut absorbiert. Aber da es auch Rotationsschwingungen ausführen kann, gibt es im Infrarot doch breitere Absorptionsbanden bei 4,3 und 15 µm.
Moleküle sind dann infrarot aktiv, wenn während der Schwingung eine periodische Änderung des Dipolmomentes auftritt. Symmetrische Moleküle aus gleichen Atomen wie O2 und N2 sind daher nicht infrarotaktiv - aber CO2 schon.

Es geht weniger um gut oder schlecht, sondern eher darum in welchem Bereich!
Die hängen von den Bindungen, Stärke, Atommassen und auch Winkeln ab, weil diese durch IR-Licht anfangen zu schwingen.
Kohlenstoffdioxid absorbiert eben genau in dem Bereich, in dem die Erde am stärksten strahlt. Der Bereich, der bei 15 °C entsteht.