Ein Gemisch aus Holzkohle und konzentrierter Schwefelsäure wird erhitzt; es entsteht unter anderem Kohlenstoffdioxid und Schwefeldioxid.?
Ich habe die Aufgabe zwar gelöst aber ich bin mir unsicher bei den Teilgleichungen, ich wusste nicht wie ich das anderes schreiben sollte bei der Reduktion. Ich finde es auch komisch, dass h2 verschwindet. Könnt ihr mich verbessern. Dankeschön
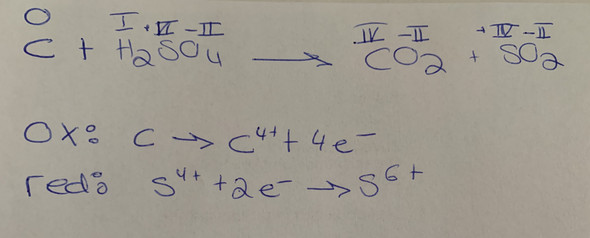
2 Antworten

Hallo wiiian
deine Teilgleichung für die Reduktion ist falsch.
Richtig ist: S⁶⁺ + 2 e⁻ → S⁴⁺
Der Schwefel wird von der OZ +6 zur Oz +4 reduziert.
Die Oxidation des Kohlenstoffs benötigt 4 Elektronen, die aus 2 S-Atomen der Schwefelsäure kommen:
2 H₂SO₄ + C → CO₂ + 2 SO₂ + 2 H₂O
Und dann erledigt sich das mit den 'verschwundenen' H's von selbst :)
LG

Das hier ist ein etwas ungewöhnlicher Fall für eine Redox-Gleichung. Wie du schon in der anderen Antwort gesehen hast, sind die Teilgleichungen nur in Bezug auf die Elektronen ausgeglichen, nicht aber bezüglich der Atom-Anzahl. Würde man dies korrekterweise machen, müsste man mit O²⁻ arbeiten. Die Teilgleichungen würden dann so aussehen:
2 H₂SO₄ + 4 e⁻ → 2 SO₂ + 2 O²⁻ + 2 H₂O
C + 2 O²⁻ → CO₂ + 4 e⁻
Teilgleichungen müssen so aufgestellt sein, dass bei dem Zusammenfassen die Elektronen herausfallen.

Woher kommt aber O^2- und H2O?? Daraus werde ich nicht schlau.. Uns wurde dies nie erklärt..!?


Die Oxidation ist die Oxidation der Kohle zum CO₂, und die Reduktion führt von der Schwefelsäure zum SO₂:
C⁰ ⟶ C⁺ᴵⱽO₂ + 4 e⁻
H₂S⁺ⱽᴵO₄ + 2 e⁻ ⟶ S⁺ᴵⱽO₂
Um daraus eine vollständige Reaktionsgleichung zu baseln, mütssen wir die untere Gleichung zweimal nehmen, damit die Elektronen herausfallen, und zum Ausgleichen noch ein paar H₂O aus dem Hut zaubern:
C + 2 H₂SO₄ ⟶ CO₂ + 2 SO₂ + 2 H₂O

Dankeschön! Habe es verstanden sehr gut erklärt!
Ich habe aber noch eine frage ich habe ja 2 mal die komplette Schwefelsäure, wenn ich jetzt die Teilgleichung für S mache beachte ich nicht, dass ich 2S habe? Oder ?