Wie sieht die Strukturformel für Blausäure aus?
Nein, ich lasse mir nicht von euch die Hausaufgaben machen, sondern ich brauche dringend Tipps. Ich habe versucht, die Strukturformel zu lösen, und auch Hinweise im Internet gefunden. Mit der Struktur Formel, die ich auf Wikipedia gefunden habe, bin ich aber noch nicht zufrieden, weil die Anzahl der Elektronen ja gar nicht aufgeht. Habt ihr vielleicht eine Idee?
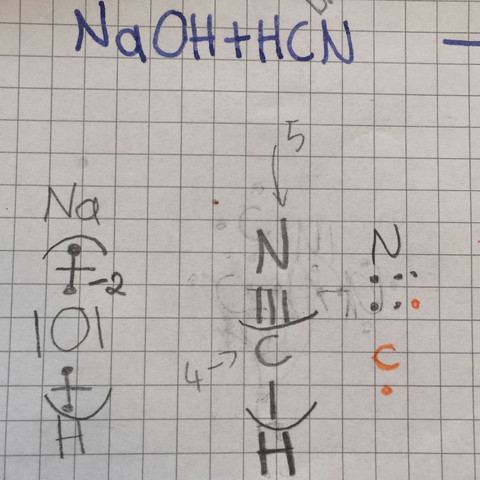
3 Antworten

Blausäure hat die Summenformel HCN(aq). Also zeichnest du zunächst ein C- Atom in die Mitte. "Rechts" zeichnest du 3 Striche, die die Dreifachbindung zum N- Atom darstellen sollen. Dem Stickstoff gibst du jetzt noch ein freies Elektronenpaar. "Links" vom Kohlenstoff zeichnest du ein H- Atom, welches du über eine Einfachbindung mit dem C- Atom verbindest.


Wobei ich Zweifel habe, dass "(aq)" hier zielführend ist.
Soweit ich weiß, ist Blausäure auch ohne Wasser stabil. OK, im Hinterkopf habe ich Polymerisationsreaktionen, aber ob Wasser dagegen hilft, ist eine andere Frage.
Und mein Hinterkopf ist sowieso eine Rumpelkammer, wo echte Schätze in einem Hauen Müll liegen.

Die Formel die du da hast ist doch richtig?! Was geht da deiner Meinung nach nicht auf?

Nein, Kohlenstoff hat 4 Valenzelektronen. Also isser 4 bindig. 3 Valenzelektronen brauchts für die 3-Facheletronenpaarbindung mit dem Stickstoff und eins bleibt für den Wasserstoff. Alles korrekt. Jeder Strich bedeutet ja 2 Elektronen.

Das klingt zwar alles logisch, aber ich stehe immer noch auf dem Schlauch. Hat N nicht fünf ValenzElektronen? Wo sind die jetzt plötzlich alle? Bei mir bleiben dann noch zwei übrig

Hat der auch, in der Konstellation hat der das gewünschte Oktett (8 Elektronen). Man lässt diese 2 Elektronen der Übersichtlichkeit halber in der Strukturformelschreibweise weg und zeichnet nur die Bindungspaare ein. Wenn du deine Formel vervollständigen willst machst du ans Stickstoffatom noch einen Valenzstrich der die 2 übrigen Elektronen symbolisiert, dann isses ultrakorrekt ;-)


H–C≡N ist schon richtig. Wenn Du es genau nimmst, dann hast Du am Sticki aber noch ein einsames Elektronenpaar, also H–C≡N|. Jetzt haben C und N ihre Oktette, und die Elektronenanzahl stimmt auch.
C hat nur zwei elektronen in der formel, aber doch eigentlich im pse 4